19 Gen 31. Le lesioni tessutali focali quali fattori patogenetici. Le basi istopatologiche ed elettrofisiologiche delle Terapie con Anestetici Locali
Claudio Dell’Anna, Massimo Barrella
Nota dell’autore.
L’Utente può prendere visione di alcuni filmati. Quelli siglati (FTI1)(FTI2)… illustrano tecniche iniettive ma non hanno finalità didattiche poiché alcune registrazioni risalgono a molti anni fa e, nel corso del tempo, molte di esse (analogamente a quanto accade in Chirurgia e nelle farmacoterapie) sono state perfezionate. Qui sono offerte in visione solo per permettere all’Utente di comprendere quanto ampio sia il ventaglio d’azione della metodica e sincerarsi del fatto che i pazienti non mostrano di patire alcuna sofferenza nel corso della loro applicazione
“…Apollo identificò Paride nel folto della mischia e lo aiutò a tendere l’arco guidando la freccia fatale.
La freccia colpì l’unico punto vulnerabile del corpo di Achille, il tallone destro, ed egli morì tra gli spasimi.”
“Etiopide” di Arctino di Mileto (VII Secolo a.C.)
L’idea del corpo umano “perfetto” è sempre stata popolare ma di non altrettanta popolarità gode l’evidenza che tanta perfezione possa deflettere a seguito di lesioni tessutali apparentemente banali, ben cicatrizzate e localizzate nella periferia somatica… oltre che l’infausto destino di Achille, erroneamente ritenuto invincibile, può venire alla mente anche l’apparente paradosso della fragilità del leone: dopo avere avuto ragione di animali anche più grandi di lui il re del Serengeti può soccombere a causa di una piccola lesione cutanea in cui una mosca abbia deposto le sue uova!
I processi riparativi post-lesionali normalmente suscitano l’attenzione del clinico soltanto in tre circostanze: allorché siano complicati da dinamiche infettivo-infiammatorie, qualora esibiscano alterazioni morfologiche in eccesso (cheloidi) o in difetto (ulcere torpide) o se si costituiscono come sede di dolore o disfunzioni locali (disturbi circolatori, problematiche biomeccaniche, eccetera). Altrimenti le cicatrici -esito naturale di ogni processo riparativo- sono considerati capitoli chiusi, oggetti di scarso interesse correlati a pregressi eventi traumatici e/o chirurgici. Perciò chi si reca a consulto da un medico che professi la Terapia Neurale secondo Huneke (TNH) può restare sorpreso che egli ricerchi accuratamente lesioni cicatrizzate di varia natura poiché ritenute possibile causa di numerose e diverse malattie e che, una volta trovate, le tratti con Anestetici Locali (AL) per contrastarne la capacità patogenetica. Ulteriore sorpresa può suscitare il fatto che oggetto di tale interesse siano anche cicatrici risalenti a tempi molto lontani rispetto all’insorgere della malattia lamentata e persino se siano topograficamente molto distanti dal distretto somatico sofferente. Ai nostri giorni se una malattia di interesse chirurgico non troppo grave prende ad affliggerci siamo abituati a pensare che incontreremo il chirurgo solo tre o quattro volte: quando emette la diagnosi, quando ci sottopone all’atto chirurgico e una volta o due dopo l’intervento per controllare che tutto sia andato bene. Invece il grande chirurgo francese Renè Leriche (1879-1955) già negli anni Quaranta del XX° Secolo aveva compreso che l’osservazione dei pazienti a distanza di tempo dall’atto chirurgico può offrire elementi di notevole interesse. Senza l’ausilio della strumentazione di indagine istopatologica di cui oggi godiamo concluse che anche quando il processo di riparazione tessutale appaia concluso “La cicatrice non corrisponde mai a un’entità morta: soprattutto nella profondità del connettivo permangono attività che possono produrre effetti indeterminati nel tempo” [63]. Sulla scorta di questo convincimento egli iniziò a indicare il trattamento con AL dei tessuti di riparazione generatori di dolore e/o di disfunzioni circolatorie e, successivamente, si spinse a raccomandare il trattamento precoce di ogni ferita chirurgica per evitare la sua eventuale trasformazione in una cicatrice “problematica”. Ma il suo intelletto acuto colse solo un aspetto della costruzione concettuale a cui gli Huneke avrebbero lavorato pochi anni più tardi: pur comprendendo che tra la realizzazione di una cicatrice e la comparsa di disturbi a essa correlabili poteva trascorrere anche molto tempo egli non giunse alla comprensione che questa può generare varie patologie anche topograficamente distanti dal distretto di origine. La TNH (metodica inclusa nella più ampia concettualità della Neuro-immunomodulazione con AL) ha espresso rilevanti risultati terapeutici in numerosi settori della Medicina Clinica e ha fondato la sua popolarità prevalentemente su una felice empiricità ma, proprio per questo, è rimasta esclusa dai principali ambiti di confronto della comunità scientifica. Il refrain che ha contribuito a questa marginalizzazione recita che essa non goda di basi scientifiche sperimentali sufficientemente robuste. Invece, dati alla mano, si può sostenere che sia vero il contrario: da decenni autorevoli ambienti della ricerca neuroscientifica internazionale che non hanno mai stabilito rapporti di colleganza con gli Huneke e con la loro “discendenza” hanno fornito alla TNH, consapevolmente o meno, solide fondamenta sperimentali. Alcune di esse saranno illustrate e discusse nelle pagine seguenti. L’obiettivo del presente capitolo è mettere in luce i più rilevanti elementi scientifici impliciti nel principale pilastro su cui la metodica si è empiricamente fondata: la capacità patogenetica delle lesioni tessutali focali e dei relativi processi di riparazione. Verranno qui affrontati i seguenti argomenti:
31a.
Panoramica sui processi biologici tessutali conseguenti a lesione focale
I processi di reazione tessutale alle lesioni focali sono stati esaminati dettagliatamente con tutte le metodologie chimico-fisiche di indagine impiegate nell’ultimo Secolo. I differenti punti di vista (biomolecolari, elettrofisiologici, morfologici, eccetera) convergono tutti univocamente a delineare un processo fondato su tre fasi:
• una prima reazione irritativa caratterizzata dal richiamo nella sede lesionale di fattori che promuovono un incremento di attività prevalentemente mediate dall’endotelio dei vasi [90][92].
• una seconda fase, “proliferativa”, in cui si assiste alla produzione di nuove strutture cito-architettoniche preposte alla ristrutturazione dell’area lesionale [71][84] che ora risulta assoggettata a una sorta di “gestione eccezionale” di funzioni nutrizionali. Normalmente dette funzioni sono governate da un ordine superiore che, in questa fase, appare temporaneamente scalzato [103]. Si tratta di un passaggio assai delicato poiché, come appresso vedremo, l’emergenza di particolari condizioni potrà determinare la capacità della lesione in via di riparazione di fungere da starter di fenomeni di “sensitizzazione nervosa” con conseguenze imprevedibili circa la localizzazione di conseguenti processi morbosi e la loro severità.
• La terza fase prevede la “regressione”: la perdita di funzionalità specifica del tessuto leso per sostituzione della trama danneggiata da parte di tessuto di riparazione. Sul piano delle sue implicazioni patogenetiche questo fenomeno, noto come “cicatrizzazione”, si mostra lungi dall’essere un problema risolto [11][33].
31b.
Processi infiammatori indotti dal “focolaio di stimoli nervosi ectopici”
Definiamo “ectopico” qualsiasi tessuto o fenomeno biologico che si manifesti in sedi diverse rispetto alla sua usuale localizzazione. E’ noto che alcuni organi (tiroide, timo, rene, eccetera) possono trovarsi nell’organismo in distretti diversi da quelli usuali e in tal caso sono indicati come “ectopici”. Il nostro interesse per i fenomeni ectopici deriva dal fatto che la Terapia Neurale secondo Huneke (TNH) contempla che gli esiti di una lesione tessutale possano esprimere i loro effetti patologici anche a notevole distanza dalla sede somatica ove essa si è realizzata. Mentre il dolore e la disfunzione articolare di una spalla a seguito di un trauma diretto a suo carico non genera sorpresa, immaginare che lo stesso quadro clinico possa scaturire da una vecchia ferita chirurgica (ad esempio) di colecistectomia pone un problema di prevedibilità della localizzazione topografica della causa e dell’effetto. Questo problema ha contribuito a diffondere intorno alla metodica degli Huneke un alone di perplessità. Nel nostro esempio la ferita chirurgica della colecistectomia si direbbe “ectopica” rispetto all’effetto a distanza che suscita poiché, secondo le aspettative comuni, il dolore e i disordini funzionali dovrebbero in questo caso interessare un quadrante dell’addome piuttosto che una spalla. Dopo questa premessa dobbiamo chiederci se la Medicina contempli l’esistenza e la tangibilità di simili fenomeni ectopici o se invece si tratti di oggetti sconosciuti alla comunità scientifica. Senza alcuna esitazione si può rispondere che la materia è del tutto pertinente alla Medicina Scientifica e, per maggior misura, che essa è stata al centro di un appassionante percorso di ricerca e di prassi clinica iniziato cento anni fa. Non illustriamo qui il contenuto delle ricerche condotte nei primi decenni del XX° Secolo da Alexandr Davidovic Speranskij [105]: se ne parlerà diffusamente altrove. Partiremo dal decennio Settanta-Ottanta di quel Secolo quando la disponibilità di nuove tecnologie per la ricerca e la mole di dati precedentemente accumulati consentì agli studiosi (molti dei quali neppure conobbero i fratelli Huneke e le loro osservazioni) di pervenire a evidenze sperimentali inoppugnabili su quelle ectopie a cui si è fatto cenno. Tra i più brillanti ricercatori in questo settore pionieri si è distinto lo statunitense Josè Luis Ochoa, attivo presso il Good Samaritan Hospital e l’Oregon Health & Science di Portland (Oregon). Dagli studi suoi, dei suoi collaboratori e di altri personaggi impegnati sulla stessa linea di ricerca è emersa la consistenza concettuale e materiale di un fenomeno, prima descritto solo sommariamente, dotato di particolari capacità patogenetiche: la Ectopic Impulse Generation (EIG) [83].
E’ intuitivo che l’insorgenza di stimoli nervosi ectopici preveda come necessaria l’esistenza di un “focolaio generatore” e presto emerse che per assolvere a questo ruolo non è neppure necessaria una vera e propria lesione anatomica: stimoli ectopici possono scaturire anche a seguito di eventi puramente funzionali attivati nei distretti più periferici del Sistema Nervoso (SN) senza che esso sia stato oggetto di alcuna lesione. I tessuti che fungono da interfaccia tra ambienti diversi dello stesso organismo e tra organismo e ambiente esterno (cute, mucose e sierose) sono tappezzati di terminazioni nervose alcune delle quali dotate di corpuscoli specializzati in relazione alla loro differenziazione funzionale. Si definiscono “noxae” gli stimoli endogeni o esogeni che risultino potenzialmente dannosi e alcuni elementi nervosi a cui, forse impropriamente, sono state attribuite funzioni di specifica propagazione della noxa sono definiti “nocicettori”: si tratta delle terminazioni specializzate nella percezione della temperatura (terminazioni amieliniche libere dette fibre C e terminazioni libere mielinizzate dette fibre A delta). Questi fungono da trasduttori di segnale poichè traducono lo stimolo fisico o chimico che perviene loro e che risulti efficace nell’eccitarli in impulsi elettrici trasmessi lungo la fibra nervosa. A causa di sollecitazioni di vario tipo essi possono rimanere sensibilizzati e, a seguito di uno stimolo pur modesto, scaricare impulsi a ritroso per un lungo periodo di tempo anche dopo che lo stimolo sia cessato. In queste condizioni si possono talora registrare scariche spontanee di impulsi a ritroso emesse periodicamente o costantemente [83]. Il modello sperimentale di sensibilizzazione dei nocicettori prevede l’applicazione di “capsaicina” (sostanza contenuta nel peperoncino) mentre condizioni analoghe si verificano spontaneamente nelle ustioni, nelle causticazioni, nelle abrasioni, negli eritemi solari e nei traumi meccanici. Per tali forme di irritazione nervosa fu coniato il termine “Angry Backfiring C-nociceptors Sindrome”che, tradotto in italiano letteralmente suona: “Sindrome dei nocicettori C irritati che scaricano impulsi antidromicamente” [23].
La sensibilizzazione dei nocicettori e l’espansione dell’irritazione nervosa nei segmenti innervati ha permesso la scoperta dell’esistenza di una fenomenologia generale, definita “Infiammazione Neurogenica”, che comprende numerose e complesse modalità di interazione tra SN e Sistema Immunitario (SI) nella genesi dei processi infiammatori. Attivando schemi funzionali propri dello stesso SN questi acquisiscono capacità di auto-perpetuazione e di auto-implementazione attraverso il coinvolgimento di un numero crescente di neuroni di differente tipo e funzione [106]. Le conoscenze che vantiamo a proposito di queste dinamiche scaturiscono anzitutto dai rilievi (storici, istologici e fisiopatologici) di un classico modello clinico e sperimentale: il neuroma da amputazione. La fibra nervosa amielinica che vi rimane coinvolta e i cui C-nocicettori siano stati a lungo sensibilizzati rilascia nel distretto corrispondente al suo campo recettivo particolari sostanze, i neuropeptidi, che di fatto si comportano come citochine infiammatorie. In particolare due di essi, la Sostanza P ed il CGRP (Peptide Legato al Gene della Calcitonina), inducono localmente edema e vasodilatazione e simultaneamente suscitano un ulteriore effetto eccitatorio sulla stessa fibra nervosa che le rilasciò alimentando così autoricorsivamente la descritta dinamica [76]. In molti casi di neurolesione periferica questo meccanismo coinvolge altri neuroni oltre a quelli inizialmente attivati: infatti iniziano a rilasciare precocemente Sostanza P anche i neuroni mielinizzati con funzione afferente in aggiunta a quelli amielinici che, tipicamente, avevano iniziato a rilasciarla già nelle prime tappe del processo [75][80][81]. Da tempo è noto che alterazioni istologiche di qualsiasi tessuto periferico (cicatrici o persino semplici incrementi della componente connettivale nei tessuti) possono generare il loop dell’infiammazione neurogenica analogamente al neuroma da amputazione. Questo dato risulta confermato e perfezionato da ricerche recentissime [7][11][34]. Il descritto meccanismo di auto-perpetuazione si realizza attraverso l’attivazione delle fibre e dei messaggeri chimici nervosi e, pertanto, non può destare sorpresa che esso ricalchi schemi funzionali propri del SN. Nel corso di lunghi decenni l’impiego empirico degli Anestetici Locali (AL) con finalità terapeutiche frequentemente ha dimostrato di poter avere ragione di patologie infiammatorie di diversa patogenesi con distribuzioni segmentarie, polidistrettuali e persino sistemiche. Tutto questo viene oggi confermato da studi condotti con rigorosa e moderna metodologia della ricerca [67][72][44]. Questa evidenza, per quanto sia ormai inconfutabile, sembra ancora suscitare perplessità in alcuni settori della comunità scientifica anche per il fatto che, fino a tempi recentissimi, gli AL non erano mai stati classificati come antinfiammatori. Le moderne conoscenze sulle modalità con cui si esprime la ricorsività dei meccanismi alla base delle infiammazioni croniche, con il ruolo cruciale che il SN vi ricopre, oggi chiariscono molti aspetti di quell’efficacia terapeutica che a lungo ha trovato difficoltà a collocarsi entro canoni dottrinari.
31c.
Dinamiche eccito-infiammatorie nell’ambito del Sistema Nervoso: la centralizzazione
Nell’ultimo decennio del Novecento venne dimostrato che, dopo qualche tempo dal verificarsi di una lesione neuroperiferica, le cellule dei gangli delle radici dorsali (“DRG”: Dorsal Root Ganglia) da cui originano le fibre interessate dalla lesione prendono a comportarsi esse stesse quale “focolaio di stimoli nervosi ectopici” [25]. Già nei primi anni Settanta del XX° Secolo era stata scoperta la presenza di leucociti nel DRG successivamente alla sezione del nervo sciatico [101]. Ricerche successive mostrarono che il Sistema Immunitario (SI) si attiva sollecitando anche i linfociti T e i macrofagi a concentrarsi nei DRG corrispondenti a un nervo periferico che solo una settimana prima era stato oggetto di lesione sperimentale [38][65]. Oltre che i neuroni direttamente interessati dalla lesione sono rapidamente coinvolti nel processo anche quelli che proiettano nella zona interessata e questo può iniziare a suggerire quanto terreno possa guadagnare una dinamica patogenetica che abbia tratto origine da una modesta lesione periferica e puntuale. Nei DRG ipereccitati a seguito della lesione della periferia nervosa numerosi piccoli neuroni soccombono [62] mentre l’espressione dei neuropeptidi (Sostanza P, CGRP, eccetera) si presenta alterata [47]. Dopo variabili latenze di tempo dall’inizio della descritta ipereccitazione dei neuroni del DRG un’altra popolazione di neuroni residente nella lamina V delle corna posteriori del midollo può, a sua volta, iniziare a esprimere un costante anomalo incremento della propria attività elettrotonica: si tratta dei neuroni multiconvergenti o “Wide Dynamic Range” (WDR). Essi possono iniziare a sensibilizzarsi già a seguito della prima fase di deafferentazione dovuta alla lesione nervosa periferica [104] e determinando l’estensione del “campo recettoriale” con possibilità di ulteriore espansione topografica del quadro clinico. In questa nuova localizzazione spinale del focolaio generatore di stimoli nervosi ectopici almeno quattro fattori oggi noti (ma è verosimile che ve ne siano anche altri) contribuiscono al suo incremento quantitativo e qualitativo: anzitutto il costante arrivo di pattern di impulsi anomali afferenti dal neuroma da amputazione o dalla lesione di un tessuto periferico innervato [14]; in secondo luogo le flessioni funzionali dei meccanismi inibitori idio- e sovraspinali GABAergici che tra l’altro spiegherebbero l’efficacia delle terapie antalgiche fondate sulla magnificazione della trasmissione GABAergica [79]; inoltre l’eventuale smascheramento di preesistenti condizioni di sub-eccitazione neuronale nel segmento interessato o in segmenti prossimi a esso [86] e, infine, la possibile convergenza di afferenze a partenza da campi recettivi controlaterali alla regione interessata per attivazione dei neuroni cosiddetti “intercommissurali” [96][58]. A proposito di quest’ultimo punto vale la pena di rammentare che negli anni Trenta del XX° Secolo il chirurgo sovietico Alexander Vasilyevich Vishnevsky, appassionato cultore di Terapie con Anestetici Locali (TAL), segnalò che il blocco monolaterale con AL della catena del sistema ortosimpatico lombare può esprimere effetti terapeutici rilevanti anche nella metà somatica controlaterale [112].
Qualunque ne sia stato il meccanismo generatore, una volta che l’ipereccitazione dei neuroni WDR sia stabilizzata mostra l’inclinazione a permanere anche dopo la rimozione del DRG [104] così che il midollo spinale assume “in proprio” il ruolo di generatore spontaneo di impulsi. In sostanza: i neuroni che ricevono il segnale dalla sorgente ectopica iniziano dopo qualche tempo a generare e a conservare a loro volta il comportamento irritativo anche quando la sorgente originaria sia stata soppressa. E’ suggestivo qui richiamare l’intuizione di una memoria nervosa per l’irritazione o, forse ancora meglio, di una memoria per l’irritazione nervosa formulata già negli anni Venti-Trenta del XX° Secolo dallo studioso sovietico Speranskij [105]. Probabilmente è per questo motivo che talora le sindromi dolorose non traggono benefici di lungo termine da molte forme di neuroablazione. Tali fallimenti terapeutici possono essere ricondotti al fatto che essa viene spesso effettuata distalmente rispetto alla sede del nuovo focolaio ectopico ma si può anche ipotizzare che anche la nuova lesione chirurgica possa a sua volta assumere le medesime caratteristiche irritative del focolaio originario. Registrazioni intraneurali in singole fibre mielinizzate hanno evidenziato anche nelle neuropatie periferiche la generazione ectopica di esplosioni di Potenziali d’Azione (PdA) spontanei, di scariche ripetitive transitoriamente interrotte da stimolazioni del campo recettivo e di scariche ripetitive innescate da un precedente PdA. Si tratta del background neurofisiopatologico dei disordini soggettivi delle sensibilità (parestesie, disestesie spontanee e indotte da stimoli) riscontrabili nelle neuropatie periferiche [17]. Recenti ricerche hanno dimostrato che la lidocaina per via sistemica può bloccare tali attività ectopiche senza alterare la normale conduzione nervosa [66][108].
Torniamo ora al percorso della “centralizzazione”. Raggiunti da quella che è un’autentica marcia ascendente degli effetti irritativi del focolaio ectopico, anche i neuroni talamici pervengono alla stessa condizione giungendo all’espressione di analoghi meccanismi di iperattività elettrica [8][21]. A questo punto la dinamica biologica è ampiamente centralizzata: seppure in un più lungo lasso di tempo si è verificata una condizione funzionalmente assimilabile a quella delle sindromi talamiche in cui (dopo eventi infartuali o traumatici) i neuroni contigui all’area necrotica entrano in stato di costante eccitazione. Successivamente le connessioni talamo-reticolari e talamo-corticali possono consentire un ulteriore incremento di complessità del quadro clinico con proiezione dei segnali irritativi verso distretti ancora più distanti [32]. Sul piano delle ipotesi patogenetiche alcuni autori sostengono che i neuroni midollari e talamici si trovano a versare in uno stato di costante eccitazione a motivo della loro esposizione alle elevate frequenze di scarica provenienti dalla periferia [94] e questo spiegherebbe come numerosi quadri morbosi, anche se ormai “centralizzati”, possano talvolta beneficiare del semplice trattamento con AL della lesione periferica secondo le indicazioni che formularono i fratelli Huneke. Normalmente la condizione di costante eccitazione dei neuroni midollari e talamici induce il loro esaurimento energetico che, in tempi variabili, si traduce nella difficoltà al ripristino del loro Potenziale membranario di Riposo (PdR) e nella facilitazione all’ingresso nella cellula di eccessive quantità di ioni calcio. A questo fenomeno, noto come “eccitotossicità” [5], segue una modificazione dell’espressione genica (Immediate Early Genes) e, successivamente, di quella fenotipica [114]. Tali aspetti epigenetici sembrano implicati nei processi globalmente connessi alla plasticità neuronale: neuroni eccitati per un certo periodo di tempo possono trovarsi a permanere indefinitamente in condizione di alterata eccitabilità anche qualora sia stata soppressa la fonte originaria della stimolazione. Tutte queste evidenze confermano che anche a livello spinale e spino-talamico i processi infiammatori e immunitari viaggiano sul filo dei segnali nervosi e che le infiammazioni neurogeniche a carico del SN possono trarre origine da focolai ectopici generati nella sua stessa compagine. Inoltre risulta confermata la possibilità che un “focolaio generatore di stimoli nervosi ectopici” (o “Campo di Disturbo”, accogliendo il lessico della TNH) esprima alcuni dei suoi effetti anche a notevole distanza dall’originario distretto generatore. Passando dal piano della ricerca sperimentale a quello della pratica clinica va sottolineato che mentre alcuni focolai generatori di stimoli nervosi ectopici sono individuabili con facilità (pensiamo ad esempio alle amputazioni falangee) altri restano misconosciuti a causa della distanza topografica che li separa dagli effetti che producono: è il caso di numerosissime cicatrici traumatiche e chirurgiche su cui, il medico che non effettui un’accurata “ricerca focale”, sorvola senza comprenderne il valore patogenetico.
31d.
Ruolo del Sistema Nervoso Vegetativo (SNV) nelle distrofie croniche e in altri processi morbosi
Il ruolo del SNV, in particolare della sua componente catecolaminergica (simpatica ovvero ortosimpatica), rimane una questione aperta. Attualmente in declino, la concezione di “irritazione nervosa simpatica” continua a proporre dati non univoci specie nei fenomeni di distrofia cronica dolorosa come le Complex Regional Pain Syndrome (20). L’evidenza che numerosi disturbi dolorosi associati a distrofia tissutale e secondari a neurolesione periferica rispondessero al blocco del traffico nervoso simpatico (ottenuto mediante simpaticectomie o applicazioni di AL) [63][12][50][52][117] ha sostenuto l’idea che la noradrenalina, rilasciata dagli assoni simpatici post-gangliari, eccitasse i neuroni afferenti primari attivando gli alfa-adrenocettori con generazione di segnali diretti al sistema nocicettivo del Sistema Nervoso Centrale (SNC). Nelle lesioni del Sistema Nervoso Periferico (SNP) un primo importante aspetto, caratterizzato da grande variabilità, è rappresentato dal numero e dai requisiti funzionali delle fibre neurovegetative che possono essere coinvolte nel neuroma da amputazione e nei conseguenti fenomeni efaptici in forza dei quali fibre nervose differenti per calibro, grado di mielinizzazione e funzione si eccitano reciprocamente [51][55]. Tutto ciò induce a considerare il neuroma da amputazione alla stregua di un’entità sinciziale neoformata. Specie per chi professi la TNH un dato estremamente rilevante è che l’ingresso della componente simpatica e la sua attivazione possono verificarsi non solo dopo lesione tronculare nel SNP ma anche a seguito di lesioni di tessuti periferici non-nervosi e questo, verosimilmente, in quanto innervati [53]. Qualunque sia la quota di fibre del SNV inizialmente coinvolte nella noxa rimane il fatto che, successivamente, nel tessuto cicatriziale prossimo al neuroma si reperta una quota non trascurabile di fibre ortosimpatiche noradrenergiche di nuova formazione [40] e inoltre è certo che la lesione di un nervo periferico innesca la germinazione ortosimpatica entro il DRG pertinente a quel nervo [74]. Tali assoni simpatici di nuova germinazione si dispongono a canestro entro il DRG attorno ai neuroni sensitivi il cui assone sia stato oggetto di lesione sperimentalmente eccitandoli ripetutamente e realizzando così un focolaio di impulsi ectopici sostenuto dal Sistema Simpatico. Questo potrebbe spiegare i casi di inefficacia del blocco terapeutico con AL, anche come misura antalgica, se effettuato sul tronco nervoso in sede prossimale alla lesione. Inoltre a seguito di una lesione neuroperiferica è possibile registrare incrementi dell’attività adrenergica nello stesso Ganglio Simpatico [67] e osservare la germinazione di assoni adrenergici nei tessuti parzialmente denervati e talora anche in quelli contigui, fenomeno questo obiettivabile nei muscoli [15], nella cute [24][26] e nelle ghiandole sudoripare [57].
E’ noto che Fattori Neurotrofici prodotti dalle cellule non-nervose della glia di un DRG sofferente (per lesione diretta o per irritazione indotta da lesione del suo tronco periferico) favoriscono lo sprouting del sistema simpatico perivascolare [122] determinando un aumento generale degli effetti adrenergici. A seguito di lesioni assonali i Gangli Simpatici esprimono un incremento di Proteine che Attraggono i Monociti e una modificazione del numero e dell’attività dei macrofagi. Lo stesso avviene nei Gangli Simpatici neuralmente connessi a DRG stabilmente eccitati [97][98]. E’ interessante cogliere come, sul piano funzionale, i messaggeri chimici che si attivano presentino due facce: i Fattori Neurotrofici rilasciati dalle cellule gliali stimolano la rigenerazione nervosa post-lesionale ma, allo stesso tempo, agiscono anche da Attrattori Chimici per i Macrofagi [60]. Per questa via essi contribuiscono all’innesco di fenomeni infiammatori “neurogenici” all’interno della compagine nervosa simpatica coinvolta nei processi riparativi delle lesioni nella periferia somatica. Se consideriamo che un Ganglio Simpatico sovrappone la sua competenza su un distretto somatico relativo a 4-5 segmenti spinali (ognuno dei quali ospita almeno un DRG) è agevole comprendere perché i fenomeni neurovegetativi consecutivi a neurolesioni possano esprimersi in settori somatici più ampi e, comunque, non corrispondenti topograficamente all’area di competenza del DRG sofferente (07b). A tale proposito va ricordato che in tutti i tessuti somatici è presente una componente sinciziale che esprime un potenziale di membrana “passivo”: essa riceve nutrimento e distribuisce le variazioni di potenziale per contiguità lungo la sua stessa estensione. La variazione di polarità globale corrisponde in ogni momento al quorum di potenziale base su cui si sviluppano i potenziali stimolo-specifici nelle cellule nervose. Nei gangli viscerali autonomici tale componente sinciziale è presente e ben sviluppata. Questa corrispondenza riflette efficacemente un concetto generale di somatotopia che vede le stazioni nervose di grado più elevato, e perciò sovrastanti la periferia tessutale, “trascinare verso l’alto” settori di quest’ultima riproducendone in forma simbolica le caratteristiche morfologiche e funzionali (07a).
Ragionando alla luce della stessa logica osserviamo che nei tessuti periferici viaggiano fibre nervose che veicolano informazioni relative a settori di spazio più o meno ampi. Una parte di queste informazioni relative a eventi periferici è trasmessa ai centri superiori in qualità di dati conseguenza-specifici e codificati in salve di Potenziali d’Azione (PdA). Un’altra quota di informazioni si estende immediatamente entro il sistema sinciziale connettivo in forma di potenziale elettrotonico sotto-soglia creando un gradiente di potenziale dal punto più vicino alla sorgente nervosa a quello più lontano che perciò risulterà relativamente iperpolarizzato. Poiché è passivamente indotto da qualsiasi sorgente depolarizzante sita al suo stesso interno, questo flusso di informazioni non è conseguenza-specifico quanto piuttosto attività-specifico: in sostanza esso rappresenta globalmente la dimensionalità spaziale e temporale degli eventi elettrici del tessuto innervato. La letteratura neuroscientifica descrive questi fenomeni definendoli “efaptici”.
Processata a livello centrale tramite archi diastaltici di vario grado di complessità, l’attività nervosa torna al ganglio autonomico con due modalità: la prima lo coinvolge alla stregua di qualsiasi altro tessuto (quindi modificandone la polarità sinciziale) mentre la seconda influenza il tessuto bersaglio attraverso un numero variabile di passaggi sinaptici dipendenti almeno in parte dalla stessa polarità sinciziale viciniore (canali ionici voltaggio-dipendenti lenti). In successivi intervalli di tempo la ritmologia delle scariche sinaptiche e dei relativi PdA viene influenzata dalle oscillazioni dei potenziali elettrotonici del ganglio che, a sua volta, costituisce la rappresentazione centralizzata delle oscillazioni del tessuto di riferimento. La comunicazione “efaptica” tra tessuto periferico e ganglio è infatti mantenuta dalla contiguità dei tessuti connettivi posti tra i segmenti periferici e i compartimenti in cui i gangli autonomici alloggiano. La descrizione della complessità di questo livello tiene in considerazione il traffico di interazioni nervose sostenuto dalla ricca rete di fibre amieliniche che avvolge le strutture parenchimatose e che è ampiamente connessa ai gangli viscerali. Attraverso la generazione di potenziali elettrotonici passivi il ganglio viscerale assume la rappresentazione centralizzata delle perturbazioni dei tessuti periferici alla stregua di “ripetitore interno” di correnti elettrotoniche sinciziali. Questa visione funzionale presenta almeno tre implicazioni. Anzitutto il ganglio viene a rappresentare un sistema integrato di trasporto di informazioni sull’attività tessutale periferica basale (interazioni trofiche, variazioni di temperatura, stimoli nocivi, eccetera) codificate in salve di PdA afferenti al SNC. In secondo luogo il ganglio viene ad assumere funzioni di tastiera su cui (tramite salve di PdA) agiscono influenze “centrifughe” che pervengono da scariche dei neuroni latero-midollari e dei centri bulbari (conseguenti a emozioni, attività reticolari circadiane, eccetera), “riflesse” (rappresentate dalla trasmissione sinaptica delle perturbazioni tessutali già processate a livelli superiori del SNC che tornano al ganglio operando il descritto confronto con le oscillazioni elettrotoniche presenti nel sistema sinciziale) e, infine, “locali” (che si manifestano con PdA sporadici frutto di sollecitazioni abnormi inserite caoticamente nel flusso oscillatorio del sistema sinciziale). La terza e ultima implicazione contempla il ganglio quale interfaccia con altri sistemi di regolazione: anzitutto quello infiammatorio-immunitario e quello che regola le caratteristiche basali del “mezzo interno” (aggregazione piastrinica, adesività endoteliale, coagulazione, regolazione dell’impiego delle risorse energetiche, accrescimento cito-istologico e differenziazione, eccetera).
Sul piano informazionale le applicazioni descritte si riferiscono a un susseguirsi di eventi in cui riconosciamo una dimensione spaziale e una dimensione temporale. La prima è data dalla rappresentazione centralizzata del ganglio mentre la seconda descrive la sequenzialità di segnapassi lenti (oscillazioni elettrotoniche) scanditi da salve di segnapassi rapidi (PdA). Ottenuta mediante la rappresentazione funzionale del sincizio periferico e attraversata dalle modulazioni nervose centrali e periferiche, la centralizzazione gangliare opera perciò come un miscelatore di infinite combinazioni tra dimensionalità spaziale e temporale delle perturbazioni che interessano il tessuto innervato. Per un approfondimento di questo modello interpretativo suggeriamo la lettura del capitolo presente in questa stessa sezione del sito “interazioni tra organismo e ambiente” (30) e la visione dei filmati “Aspetti ineludibili di neurologia: la computazione nervosa” (FEF1), “Le complicanze croniche post-traumatiche e post-chirurgiche” (FEF2) e “Aspetti architettonici e fisiologici delle vie nervose afferenti e fondamenti della neuromodulazione” (FEF3) tratti dai nostri seminari del Novembre 2018 e del Giugno 2019.
31e.
Il moderno concetto di “sensitizzazione”.
Il termine “sensitizzazione centrale” è attualmente utilizzato nell’interpretazione patogenetica di numerose sindromi mio-fasciali, della fibromialgia, del colon irritabile e della vulvodinia [119], quadri morbosi in cui la componente immunologica è scarsamente rilevabile. Dal punto di vista strettamente elettrofisiologico la “sensitizzazione” consiste nel deragliamento del codice di trasduzione analogico-digitale di una o più unità nervose. Per comprendere il senso di tale affermazione occorre pensare a una delle prime caratteristiche della funzionalità della cellula nervosa: usando una grossolana affinità con l’elettronica essa è un “trasduttore analogico-digitale”. Qualsiasi grandezza fisica variabile nel tempo è una misura analogica descrivibile come la variazione di un numeratore che reca il parametro rappresentativo della sua entità (a) rispetto al flusso del tempo (T): ″Δa/T”. In Fisiologia è descritto un modello molto semplificato di trasduzione digitale della variabile Δa/T come “trasduzione da recettore tonico proporzionale”. In altri termini il recettore nervoso induce nel neurone l’emergenza di una scarica di Potenziale di Assone (PdA) p (valore discreto in unità digitale 0 – 1 in quanto non variabile sul piano dell’intensità) la cui frequenza (PdA/tempo, Δp/T=f) è direttamente proporzionale alla variazione dello stimolo analogico nel tempo: f/Δa x 1/T. Sperimentalmente questa relazione è esprimibile da un preparato di un neurone gangliare il cui recettore sia stimolato con una sorgente analogica adeguata alla sua modalità (ad esempio, misura di stimoli meccanici espressi in Newton su un recettore periferico di Merkel) [13] e venga simultaneamente registrata la scarica di frequenza emergente dal “monticolo assonico”, cioè dal settore di neurone deputato alla generazione dei PdA. Grazie a questo modello di misura la ricerca algologica di base cominciò a evidenziare fenomeni elettrofisiologici strettamente connessi all’esposizione delle fibre nervose ad ambienti caratterizzati da stimoli nocivi (come l’insulto ischemico o i traumi meccanici). Già si è accennato alla comparsa del focolaio di stimoli ectopici rappresentato dal neuroma da amputazione quale espressione del rimaneggiamento morfofunzionale post-traumatico di un segmento nervoso. Anche nella periferia “non-nervosa” (ma in ogni caso innervata) il fenomeno iniziale che si verifica nell’interfaccia tra spazio intercellulare e terminazione nervosa di un tessuto si traduce in ogni caso in una iperstimolazione nervosa, sia essa derivante da un eccessivo incremento dello stimolo adeguato (come l’eccesso di pressione o di temperatura), sia essa effetto di fenomeni biochimici indotti dalla lesione tessutale (abbassamento del pH, produzione di cataboliti citotossici, interruzione della fosforilazione ossidativa). Indipendentemente dalla specifica struttura istologica in cui questo avviene e dall’origine fisico-energetica dello stimolo induttore si verifica un incremento del numeratore nel rapporto f/Δa x 1/T prodotto dai neuroni afferenti del corrispondente tessuto innervato. In altre parole è come se il corrispondente campo recettoriale, costituito da vie afferenti normalmente ripartite e segregate in classi di fibre aventi ciascuna un diverso “range” di frequenza di scarica, venisse inondato da altissime frequenze di scarica tendenzialmente superiori alla capacità di contenimento nell’ambito di quel campo recettoriale. A ciò consegue l’abbassamento della soglia d’eccitazione delle fibre coinvolte [20][102], l’estensione del campo recettoriale oltre i propri limiti spaziali [36] e infine ne risulta deformata la specificità modale delle sensazioni che vengono dirottate verso vie afferenti che presentano maggior quota di reticolarità: le vie multisinaptiche [18][120]. Accogliendo la validità di questo modello generale di produzione della sensazione dolorosa diventa più agevole intuire il processo della cronicizzazione del dolore quale fenomeno di natura disadattativa: invece di attivare un processo di inibizione diretta del fattore f/Δa (ovvero un fenomeno di adattamento) l’istanza di assorbire l’eccesso di f/Δa x 1/T può assumere la vocazione ad alterare consensualmente la struttura e l’architettura nervosa del campo recettoriale [19]. Già negli anni Trenta del XX° Secolo Speranskij aveva compreso che dopo una lesione della materia nervosa o di un settore della periferia somatica innervata la sensibilità del SN agli stimoli muta contestualmente alla trasformazione dell’architettura interna delle strutture biologiche implicate [105]. Non si comprende pertanto come questo dato ancora non sia riuscito a guadagnare il meritato interesse quando analoghe evidenze relative al Sistema Immunitario (SI) da tempo costituiscano patrimonio fruito e indiscusso: sulle modificazioni interne del SI a seguito di stimoli antigenici e neuro-endocrino-immunologici si basano infatti numerose diagnosi e si tracciano altrettanto numerose strategie terapeutiche. Tornando al SN i citati fenomeni di abbassamento della soglia d’eccitazione, estensione del campo recettoriale e deragliamento della specificità modale tenderanno a mantenersi manifestandosi clinicamente attraverso l’iperpatia, l’estensione dell’area dolorifica e l’allodinia, cioè attraverso quelli che oggi vengono riconosciuti “sintomi stigmate” (hallmarks) della sensitizzazione.
Si definisce sensitizzazione “primaria” il processo che, presentando le caratteristiche appena descritte, si realizza tra la periferia tessutale e il recettore del neurone afferente primario (il primo neurone di senso). La sensitizzazione “secondaria” si verifica nelle successive stazioni sinaptiche afferenti fino al raggiungimento delle sedi encefaliche (sensitizzazione “centrale”). L’avvìo della sensitizzazione primaria crea le condizioni per il determinarsi della sensitizzazione secondaria fino allo stadio della sensitizzazione centrale [109].
31f.
Sensitizzazione e Fattori di Crescita: un rapporto di regolazione biunivoca
Il “neurotrofismo”, ovvero la relazione tra l’innervazione e la struttura istologica dei tessuti, rappresenta un patrimonio di conoscenze piuttosto antico. Costituisce un consolidato bagaglio culturale il fatto che la denervazione dei muscoli comporti la degenerazione delle miofibrille fino alla loro sostituzione fibroconnettivale al di là della validità dell’apporto metabolico per via ematica [35][4]. Successive ricerche hanno evidenziato ancora più nettamente come la sostituzione dell’innervazione muscolare da parte di diverse classi di motoneuroni induca una corrispondente conversione delle caratteristiche morfo-funzionali delle fibre muscolari [87]. L’apogeo della ricerca più recente circa il neurotrofismo si espresse tuttavia negli anni Novanta del XX° Secolo con la scoperta dei Fattori di Crescita, in particolare il complesso delle Neurotrofine e del Nerve Growth Factor (NGF) [3] che troviamo espressi per lo più a seguito di lesioni della materia nervosa e/o dei tessuti innervati. Attraverso quali meccanismi si verifica l’interazione tra i Fattori di Crescita e la variazione del fattore f/Δa espresso dai neuroni afferenti nel processo di sensitizzazione? Il più potente regolatore del rapporto f/Δa è rappresentato dalla densità ed eterogeneità degli effettori del PdA: i Canali Ionici trans-membrana (CI) sia voltaggio-dipendenti che non [107]. Negli ultimi decenni l’accumularsi di sempre nuove acquisizioni ha conferito a questo tema un notevole livello di complessità (33). L’aspetto che qui preme rimarcare è che, alla luce delle recenti conoscenze bio-molecolari, tutti i sistemi di regolazione (endocrinologico, immunitario e nervoso) direttamente o indirettamente risultano implicati nella modulazione dell’attività dei CI transmembranari delle cellule nervose. L‘organizzazione strutturale e l’architettura dei CI transmembranari di un neurone è funzionale alla regolazione di un parametro “finale” fondamentale: il periodo refrattario. Elettrofisiologicamente esso corrisponde a quel grado di iperpolarizzazione di un punto della membrana che rende impossibile in quel dato momento la produzione di un PdA e, in sostanza, costituisce il “segnapassi” che regola il range di frequenza di scarica per ogni tipo di neurone. La regolazione in termini di intensità e durata di questo segnapassi corrisponde alla regolazione dell’intera capacità informazionale della cellula nervosa all’interno della sua rete di scambio. Tra le numerosissime interazioni che determinano la variabilità della generazione del periodo refrattario in una cellula nervosa c’è la stessa attività di scarica nel tempo (ciò che chiamiamo “firing”): da decenni è noto che i fenomeni di attivazione voltaggio-dipendenti dei CI transmembranari sono in grado di influenzare la generazione del periodo refrattario in misura relativamente indipendente da altri fattori di modulazione [111]. Questa potenzialità di autoregolazione costituisce uno dei meccanismi strutturali del processo di adattamento sensoriale, ossia la riduzione del rapporto f/Δa. Già si è accennato alla capacità delle scariche efaptiche scaturite dal moncone nervoso dopo lesione completa (neurotmesi) di indurre processi ricorsivi di rimaneggiamento strutturale del neurone lesionato. Anche se la relazione tra la produzione di attività elettrica e la modulazione di Fattori di Crescita è materia approcciata dalla ricerca biomolecolare solo da pochi anni già disponiamo di numerose conoscenze sul ruolo dei campi elettrici endogeni suscitati dai tessuti lesionati. La produzione di campi elettrici è stata accertata quale iniziale e principale fonte di guida per la costituzione architettonica dei processi riparativi: essa fungerebbe da vera e propria “linea di orientamento” della distribuzione temporo-spaziale dei Fattori di Crescita entro le popolazioni cellulari [73]. La coniugazione tra fenomeni elettrici ed eventi biochimici viene così a costituire una chiave interpretativa universale dei fenomeni di rimaneggiamento dei tessuti nei viventi in relazione alle continue perturbazioni esterne. Ovunque si presenti un fenomeno di firing eccessivo e continuativo di natura biologica (ad esempio indotto da un fenomeno efaptico) oppure apportato artificiosamente dall’esterno (tramite stimolazione elettrica) si registra la tendenza alla produzione/modulazione di molteplici Fattori di Crescita attivi su svariate linee differenziative cellulari. Già sono note molte delle dinamiche che inducono la sensitizzazione primaria delle terminazioni nervose della periferia attraverso l’azione dei Fattori di Crescita Neurotrofici. La più studiata è rappresentata dall’aumento della densità dei CI rapidi voltaggio-dipendenti del sodio entro la membrana assonale [45][85]. Nuovi dati sono emersi circa i Fattori di Crescita che consensualmente inducono trasformazioni post-lesionali di molteplici popolazioni cellulari e tessuti connettivi (Vascular Endothelial Growth Factor, Fibroblast Growth Factor, Transforming Growth Factor, eccetera), ovvero di tutti i costituenti del campo recettoriale innervato. In altri termini, la sensitizzazione quale fenomeno bioelettrico della membrana nervosa e la modulazione dei Fattori di Crescita che lo sostengono sono eventi che non possono essere considerati separatamente: il versante elettrico e quello biochimico rappresentano infatti le due facce di un unico processo poiché la stessa sensitizzazione (intesa come modificazione disfunzionale del tessuto innervato) è il presupposto plastico per la successiva deformazione della sua struttura cito-architettonica (distrofia neurogena) da parte dei Fattori di Crescita extranervosi attivati dal processo [16][30]. Quale evento cruciale della cronicizzazione patologica il processo di sensitizzazione assume in questa luce un significato assai più ampio e suggestivo: l’inferenza continuativa nel tempo da parte della noxa può indurre un fenomeno adattativo che, partendo dal deragliamento verso l’alto del firing nel campo recettoriale, cerca un nuovo equilibrio morfologico ed energetico attraverso la sua deformazione spaziale conseguita tramite la modulazione di diversi fattori di crescita agenti su diverse linee differenziative cellulari.
31g.
Plasticità dell’innervazione tessutale
Recenti nozioni permettono di delineare un modello di regolazione immunitaria del neurotrofismo: a ogni processo di perturbazione dell’innervazione dei tessuti, attraverso l’attivazione di citochine immunitarie e di Fattori di Crescita, si inducono al tempo stesso la modulazione/differenziazione di cellule immunocompetenti e la stimolazione della plasticità del neurone [77]. Quest’ultima si articola su diversi stadi: quelli iniziali corrispondono a deviazioni delle caratteristiche funzionali della membrana neuronale (come la sensitizzazione o l’adattamento) mentre gli stadi avanzati corrispondono alla diversificazione dell’arborizzazione delle terminazioni dei singoli neuroni con radicale e irreversibile mutamento delle caratteristiche informazionali dei circuiti nervosi e, quindi, della qualità globale delle interazioni tra organismo e ambiente. Alla luce delle nuove conoscenze sui Fattori di Crescita e sul loro ruolo nel promuovere la sensitizzazione ciò che è stato prima accennato rispetto ai processi patogenetici connessi al neuroma da amputazione assume il carattere di un paradigma interpretativo: l’insieme dei fattori implicati (anzitutto la loro dinamica temporale) descrive la vita dell’individuo come la storia di un incessante rimaneggiamento morfo-funzionale della sua periferia innervata sollecitato dalle interazioni ambientali tramite la mediazione della risposta infiammatoria. Quest’ultima assume il ruolo di costante promotore della plasticità dell’organizzazione istologica ove detta plasticità è impersonata dalle continue modificazioni architettoniche della loro innervazione. Una volta che siano correttamente collocati nello spazio e nel tempo i fenomeni interattivi dell’organismo assumono rispettivamente una dimensione architettonica tridimensionale e un andamento oscillante. Il come, il dove e il quando l’evento patologico si propone in un nuovo formato non sono più semplicemente interpretabili quali errori del dosaggio di alcuni ingredienti del brodo della biochimica o, all’opposto, quali variabili entro il campionario di malfunzionamenti di un giocattolo meccanico. Il continuo passaggio tra salute e malattia ci appare quale effetto di un incessante susseguirsi di eventi infiammatori (suscitati dall’interazione con l’ambiente) che, durante tutta l’esistenza, inducono modificazioni plastiche, funzionali e strutturali di più distretti tra loro connessi. Qualora dette modificazioni esitino in una riorganizzazione dei tessuti innervati in grado di accogliere le istanze inibitorie anti-infiammatorie la malattia potrà esaurirsi anche se, alla fine, l’organismo risulterà “cambiato” (come quei soggetti che a lungo restano asintomatici ma pronti a sviluppare una micidiale anafilassi a una successiva puntura di vespa) o, più genericamente, “invecchiato”. Altre eventualità sono rappresentate dalla sopravvivenza al costo della cronicizzazione della patologia per delimitazione di un “sistema autopoietico”, ovvero di un circolo vizioso locale [113], o il decesso per diffusione dell’infiammazione all’intero organismo.
31h.
Sistemi di organizzazione anatomo-funzionale infraspinali
Il fulmine ideativo che condusse Alfred Pischinger a formulare il concetto di “Sistema-Ambiente di Regolazione Cellulare di Base” (SARCB) scaturì dal riconoscimento istologico di terminali nervosi amielinici entro lo spazio intercellulare (interstiziale) [89]. Fino a quel momento regnava la convinzione che la presenza di una terminazione nervosa fosse sinonimo esclusivo di integrazione somato-motoria di livello spinale. La sorprendente eccezione derivò dall’evidenza che in quella sede la posizione della terminazione nervosa non fosse connessa a una specifica modalità sensoriale o motoria ma venisse a rappresentare una sorta di spettatore aspecifico in una dimensione ubiquitaria e indifferenziata: una quota di materia nervosa reticolare priva di qualsiasi focalità e di qualsiasi specificità funzionale. In quella veste inedita il Sistema Nervoso (SN) non esibiva le note caratteristiche di struttura gerarchicamente organizzata ma entrava in commistione funzionale con quanto di più aspecifico risiede nella periferia di ogni tessuto: secrezioni delle cellule fibro-connettivali, immunoglobuline in vario stato di attività, processi citolitici indotti dalla liberazione di enzimi, ormoni, eccetera. Questo adduceva la prova istologicamente inconfutabile dell’esistenza di un settore di SN del tutto indipendente da quella pietra angolare della fisiopatologia nervosa del Novecento rappresentata dal riflesso segmentario spinale identificato da Sherrington: l’attore (mai comparso prima sulla scena) di una forma di regolazione non soggetta alla necessità di una ricerca puntuale dello stimolo localizzato. Quelle straordinarie rilevazioni istologiche non mancarono di aprire interrogativi sul significato di una simile forma di regolazione nervosa inscritta in un sistema “autopoietico” che, di fatto, può anche fare a meno di livelli superiori di integrazione. Nel corso degli anni alcune importanti risposte sono pervenute dalle conoscenze sulle interazioni tra l’attività bioelettrica dell’innervazione tessutale e il trofismo degli stessi tessuti. Il concetto di trofismo è assai estensivo poiché in una sola parola esprime una conformazione geometrica tridimensionale di una struttura (ad esempio, un organo) ma anche la sua capacità di mantenersi costante mediante un corretto corteo di scambi enzimatici energicamente validi. In ossequio ai principi di Virchow, se assumiamo che tutte le perturbazioni vigenti all’interno di un tessuto pluricellulare siano ascrivibili esclusivamente a un disordine della cellula che di quel tessuto è “dominante” (fibrocellula rispetto al tessuto connettivo, cellula epiteliale rispetto al tessuto mucoso, eccetera) non giungiamo alla comprensione dei possibili ruoli dell’innervazione del sistema interstiziale. Dovremmo infatti arroccarci sulla convinzione contraddittoria che tutte le alterazioni patologiche siano causate esclusivamente dalla sofferenza della cellula, al tempo stesso effettrice di una funzione specifica e garante della produzione e della manutenzione dell’aspecifico tessuto circostante. Nonostante la sua apparente affidabilità nella valutazione dei processi fisiologici il limite della visione virchowiana emerge invece con grande chiarezza nei fenomeni patologici: nel corso di qualsiasi patologia intercorrente (sia essa infiammatoria, neoplastica o ischemica) il primo passaggio che si manifesta nel produrre la malattia d’organo non è la sofferenza cellulare quanto piuttosto l’alterazione dell’ambiente in cui la cellula “specializzata” si trova immersa: l’interstizio.
Per chiarire questo concetto dobbiamo combinare i fenomeni connessi alla disposizione architettonica delle strutture tissutali (strutture longitudinali, circolari, orientamenti in direzione di un gradiente di flusso) con le dinamiche biomolecolari che governano tali disposizioni nell’ambito dell’organismo. Questo studio della geometria dei costituenti tessutali entra in rapporto obbligato con l’osservazione delle proprietà elettrostatiche ed elettromagnetiche degli stessi anche nei modelli sperimentali più semplici (come quelli basati unicamente sulle interazioni che avvengono tra polimeri immersi nell’acqua). Da decenni ci si ostina a separare i fenomeni biochimici, ossia strettamente enzimatici, dagli eventi elettrofisiologici che vi si ritrovano indissolubilmente associati già a partire dal trasporto ionico di elettroni che accompagna qualsiasi trasferimento molecolare (pensiamo alla ossido-riduzione). Questo rende assai difficile concepire il significato fisiologico di un fattore, come quello fornito da un produttore di sequenze di impulsi elettrici all’interno del compartimento interstiziale ove vige apparentemente solo uno scambio di nutrienti e fattori enzimatici tra cellule affrontate l’una all’altra. In realtà è disponibile una ponderosa letteratura scientifica sul ruolo della “elettricità endogena” nel governo dei fenomeni differenziativi e adattativi tessutali [9][29][46][99][118]. Il primo ostacolo allo sviluppo di questo filone di ricerca è rappresentato dalla necessità di studi in vivo, visto che nelle metodiche di analisi su colture cellulari in vitro si sconta proprio la mancanza dell’innervazione interstiziale. Questo importante deficit metodologico è stato segnalato anche in altri settori di questo sito.
L’intervento combinato di diverse modalità di interazione (enzimatiche, infiammatorie e ormonali) che aggettano su un ambiente omogeneo come lo spazio interstiziale implica sul piano informazionale l’elaborazione di messaggi unitari che assumano la forma di “simboli”. Questi esprimono le combinazioni di eventi perché vengano raccolte e interpretate dalle stazioni superiori senza dover riprodurre le medesime condizioni fisico-chimiche di partenza a ogni passaggio gerarchico d’informazione. Solo in questa luce è possibile intuire la funzionalità del SN inserito nello spazio interstiziale: la cellula nervosa assolve all’unica funzione di convertire in sequenze di PdA le perturbazioni biolettriche provocate dagli eventi chimici e convogliare le sequenze di potenziali attraverso il proprio asse di propagazione. Sequenze di PdA vengono così a rappresentare la simbolizzazione codificata di combinazioni di fenomeni interstiziali accomunati dalla capacità di stimolare la terminazione nervosa aggettante. La convergenza di più terminali nervosi su una successiva stazione di recettori dei gangli autonomici (inseriti in un ambiente simile all’interstizio ma altamente selettivo e puntiforme qual’è quello della sinapsi) rappresenta il successivo livello gerarchico di elaborazione delle informazioni che, per livelli successivi di integrazione, giunge fino ai nuclei afferenti vegetativi del tronco encefalico.
Prima di soffermarci su questi livelli informazionali di ordine superiore è importante precisare gli aspetti strutturali e funzionali della loro fonte, ovvero ciò che Pischinger definì “SARCB” (in letteratura si trova frequentemente il termine “Zelle-Milieu Sistem” = ZMS). L’elemento copernicano che in esso è implicito non sta solo nel suo riconoscimento di insieme costituito dalla cellula, dallo spazio intercellulare, dall’endotelio vascolare e dalla terminazione amielinica ma anche (forse soprattutto) nel fatto che in risposta a diverse perturbazioni tutti i citati elementi sono in grado di suscitare reciprocamente modificazioni strutturali tali da variarne consistenza e disposizione geometrica. Così la risposta del ZMS di qualsiasi distretto somatico a una improvvisa riduzione del rifornimento di nutrienti e di ossigeno (come avviene nell’ischemia locale) comporta:
- la pronta modificazione della struttura cellulare sia in termini di geometria della cellula nel suo insieme che in termini di struttura e disposizione dei compartimenti intracitoplasmatici [95]
- il cambiamento della composizione del materiale biologico intercellulare in termini di composizione biochimica dei costituenti della sostanza connettivale ove questo coincide con il deragliamento dell’osmolarità, della capacità di legame con l’acqua, del gradiente bioelettrico acido-basico, del potenziale redox e della acquisizione di una morfologia fusiforme o circolare [39][1][10][121]
- la variazione della permeabilità di membrana e della disposizione architettonica delle cellule endoteliali per favorire il passaggio di liquido dal compartimento intravascolare [2]
- la variazione del gradiente di eccitabilità della terminazione nervosa aggettante nel ZMS attraverso l’assunzione di una deviazione morfo-strutturale della distribuzione dei CI membranari voltaggio-dipendenti. Tale deviazione realizza la cosiddetta “inward rectification”: un maggiore range di frequenza di scarica per unità di stimolo [6][64].
Questi fenomeni avvengono pressoché simultaneamente quali risposte tissutali standard all’ischemia in modalità relativamente indipendenti dal tipo di specializzazione d’organo, suscitati da stimolazioni “a domino” esercitate da ciascun elemento costitutivo del ZMS sull’altro: le cellule bisognose di nutrienti secernono sostanze intracellulari nell’interstizio che alterano il tessuto connettivale sia degradandolo sia richiamando altre cellule e queste ultime passano attraverso le cellule endoteliali a loro volta sollecitate a separarsi. Il tessuto connettivale alterato deforma la geometria delle relazioni tra cellule estendendo il compartimento bioelettrico comune secondo linee di propagazione corrispondenti alla nuove conformazioni tridimensionali delle molecole del connettivo interstiziale (glicosaminoglicani, proteoglicani, eccetera) e proponendo gradienti di formazione di potenziali elettrotonici su aree volumetriche più estese e geometricamente deformate. A loro volta queste nuove conformazioni tridimensionali di campi elettrostatici inducono la facilitazione transmembrana della depolarizzazione nervosa a intensità crescenti su un maggior numero di terminazioni amieliniche. Dal canto loro queste facilitano la progressione dei processi di degranulazione cellulare, di permeabilizzazione dell’endotelio e di richiamo di cellule dal torrente circolatorio sui volumi interstiziali così architettonicamente deformati. Questi processi a cascata simultanea, da decenni oggetto di ricerca in Patologia Generale, sono talmente interconnessi da rappresentare un fenomeno unitario. Lo spegnimento della cascata avviene per il successivo intervento di fattori, indotti dalle medesime conseguenze dell’alterazione iniziale, per cui la rappresentazione storica dell’evento ischemico focale finisce per abbracciare l’intero arco temporale: dall’accensione del processo fino alla strutturazione dell’esito fibrocicatriziale [41][37][31][78][42][88][91][100].
Nella valutazione dei fenomeni reattivi del ZMS l’interesse primario di Pischinger si orientò principalmente sull’applicazione di questo modello anatomo-funzionale fondamentale nella teoria dell’omeostasi energetica [89]. Il riconoscimento di dinamiche di autodistruzione cellulare (soprattutto leucocitaria: la leucocitolisi) quali fenomeni attivi esercitati dal sistema vivente sottoposto a stress patologico lo condusse a suggestive intuizioni rispetto alle capacità dell’organismo nel salvaguardare il proprio generale stato di salute energetica attraverso processi biologici che oggi potremmo avvicinare al moderno concetto di “apoptosi”.
31i.
Rappresentazione centrale del “Zelle-Milieu Sistem”(ZMS)
Se consideramo le citate potenzialità anatomo-funzionali di una possibile proiezione nervosa afferente del ZMS in termini di “campo recettoriale” (cioè entro il dominio spaziale) emerge l’esigenza di coglierne anche alcune delle caratteristiche temporali, anzitutto quelle legate alla trasmissione di interazioni lungo percorsi che attraversano l’organismo. Le caratteristiche temporali di queste trasmissioni sono esprimibili in due termini:
- la velocità, ossia la distanza coperta da una leva funzionale (“vettore”) nell’unità di tempo
- la geometria, ossia il percorso compiuto dal vettore nell’ambito della compagine tridimensionale del tessuto.
Le leggi fisiche che regolano la propagazione dei vettori biologici sono le stesse che regolano i processi inorganici. Nei sistemi viventi l’aspetto che cambia è che essi mettono in atto modificazioni che fanno variare tali leggi attraverso modificazioni della propria struttura. Un esempio è il meccanismo di reazione allosterica che avviene nell’interazione tra molecole reagenti in risposta all’azione enzimatica: la facilitazione dell’interazione chimica, che a data temperatura ambientale necessita di altissime concentrazioni di molecole reagenti (numero di particelle x pressione atmosferica) avviene a temperatura ambiente e a pressione stabile perché l’enzima preposto assume una conformazione geometrica particolare (dominio) che agevola l’incontro tra le molecole attivando una via preferenziale. Quando queste conformazioni enzimatiche variano tra stati geometrici alternativi (allosterici) l’enzima assume le caratteristiche informazionali di un interruttore che agevola o inibisce tale reazione chimica. Probabilmente nell’evoluzione dei vertebrati il modello di regolazione per dominio allosterico più importante è quello dell’emoglobina: la sua capacità di legare l’ossigeno nei polmoni e trasportarlo in periferia per cederlo ai tessuti è fornita dal suo gruppo prostetico (“eme”) autoregolato dalla stessa concentrazione extracellulare di ossigeno: laddove quest’ultima è alta, come negli alveoli polmonari, l’eme dispone l’enzima in una conformazione geometrica che facilita il suo legame con l’ossigeno mentre laddove questa si abbassi la stessa emoglobina assume caratteristiche geometriche opposte favorendone la cessione ai tessuti periferici. Dal punto di vista biocibernetico l’intero processo di trasporto dell’emoglobina assume il ruolo di vettore di una sostanza altrimenti ubiquitaria, come l’ossigeno, in una dimensione temporale attraverso un “flusso”. Nell’esempio del trasporto d’ossigeno il flusso, inteso in termini di velocità e geometria di propagazione, si distingue in due grandi compartimenti: interstiziale (sottoposto al dominio proprio della sostanza di regolazione di base) e intravascolare (sottoposto a un dominio gerarchicamente superiore). Nel primo dominio il flusso possiede infatti una direzione trasversale (nello spessore di sostanza intercellulare tra cellula d’organo e cellule endoteliali), diffusa e lenta, “capillare”. Nel secondo dominio, cioè nel vaso sanguigno, il flusso assume una direzione longitudinale, “idraulica”, localizzata (laddove si sfiocca la ramificazione vascolare o dove arriva il ramo terminale arterioso) e rapida, poiché spinta dalla forza della sistole cardiaca. A questo punto va enfatizzato che tra il primo e il secondo dominio una differenza fondamentale risiede nella densità di scambi del vettore tra ambienti contrapposti: nell’ambiente intercellulare la densità è massima perché gli scambi si svolgono in ogni punto di contatto tra interstizio e cellula (massima reticolarità) mentre nell’ambiente intravasale la densità di scambi è minima perché il flusso di sostanza percorre lunghe distanze attraverso i tessuti protetto dalla superficie endoteliale che è chiusa rispetto all’interstizio circostante (minima reticolarità). Bisogna ammettere che potrebbe apparire schematico parlare di due compartimenti distinti e di dominio superiore: tra questi due poli estremi si situa infatti una gamma di situazioni strutturali intermedie che vanno dalle anastomosi artero-venose alle reti mirabili fino ai sistemi portali. Ciascuna caratteristica architettonica peculiare permette di sfruttare le stesse leggi fisico-chimiche del sistema circolatorio per ottenere delle variazioni di flusso informazionale utili a particolari funzioni biologiche. Ciò che è importante rilevare è che la regolazione funzionale dei flussi informazionali avviene sempre e soltanto attraverso la modificazione, più o meno reversibile, delle caratteristiche strutturali che regolano il percorso del vettore. Così, in relazione a perturbazioni locali o sistemiche fisiologiche o patologiche, il flusso dell’emoglobina può trovare avanti a sé l’incremento del percorso nel compartimento interstiziale attraverso l’aumento delle sue dimensioni e/o della sua componente acquosa mentre, al contempo, la riduzione della quota di percorso longitudinale corrisponderà all’incremento di reticolarità della geometria vascolare per l’apertura degli sfinteri pre-capillari collaterali. Tutto questo avviene, ad esempio, in corso di infiammazione acuta. Dal punto di vista della funzione dell’emoglobina il risultato è il maggiore intervallo di tempo trascorso da parte di una certa quota di sangue nella condizione che allostericamente corrisponde al rilascio di ossigeno ai tessuti. La conseguenza è l’incremento di cessione di ossigeno dal sangue ai tessuti periferici infiammati. Fenomeni di segno opposto (o diversamente articolati) si verificano in diversissime condizioni, fisiologiche o patologiche, che tuttavia coinvolgono i medesimi sistemi di regolazione: la vasocostrizione degli sfinteri pre-capillari del derma associata alla lipolisi del tessuto connettivo durante l’esposizione al freddo, l’apertura degli shunts arteriolo-venosi associata all’incremento del flusso vascolare in corso di malattie infiammatorie connettivali, il depauperamento della rete arteriosa associato all’ispessimento della sostanza connettivale nelle fasi avanzate dei processi infiammatori e delle patologie vasculo-ostruttive sono altrettanti esempi di come la regolazione del compartimento individuato nella sostanza di regolazione di base sia strettamente associata alla regolazione del suo dominio immediatamente superiore: quello della circolazione intravascolare. L’esempio dell’emoglobina come leva funzionale è particolarmente illuminante rispetto alla modalità con cui i costituenti del sistema di regolazione di base vengano a loro volta deviati dallo stesso vettore su assetti funzionali variabili: nel caso succitato dell’infiammazione il risultato di una maggiore estrazione di ossigeno tra polo arterioso e polo venoso nell’ambito di un circoscritto distretto tessutale tende a impoverire la disponibilità di ossigeno nei distretti circostanti. Questa relativa ipossiemia circostante all’area infiammata provoca un’immediata sofferenza metabolica delle cellule viciniori che si traduce in un calo del pH. Quest’ultimo, tramite altre leve funzionali (bradichinina, ossido nitrico, eccetera) provoca ulteriore ingrandimento e deformazione dello spazio interstiziale. L’estensione dell’area tessutale infiammata (nonché la disposizione circonferenziale di aree in cui vengono a trovarsi contemporaneamente diversi assetti microcircolatori alternando aree concentriche di iperemia e di vasocostrizione capillare) è frutto di fenomeni reiterativi che possono sollecitarsi reciprocamente entro variabili tempi ed estensioni topografiche fino a esaurirsi. Se in questo contesto inseriamo gli effetti derivanti da tutti gli altri attori del ZMS (l’ingresso di cellule infiammatorie per diapedesi, la deformazione dei componenti polimerici della sostanza interstiziale, la degranulazione e la distruzione delle cellule parenchimali, l’intervento di sostanze ad azione ormonale) il livello di complessità del quadro assume dimensioni enormi. Ciascuna leva funzionale si riferisce infatti a un suo proprio flusso informazionale connesso a meccanismi regolatori, sia locali che remoti. Ciò che si intende sottolineare è che il ZMS, almeno per come descritto da Pischinger, non rappresenta una piattaforma omogenea su cui sostano gli effettori regolatori (ormoni, agenti infiammatori, nervi) ma un mosaico magmatico che si plasma e si riorganizza continuamente in relazione agli eventi esterni in una fusione sinergica con altri attori, a loro volta disposti su domini di flusso funzionalmente e anatomicamente sovrapposti. Diviene così facile comprendere come, in occasione di eventi interattivi acuti (ischemia, infiammazione-infezione, trauma, eccetera) si attivino contemporaneamente molteplici flussi informazionali che scorrono ciascuno seguendo il proprio dominio spazio-temporale (intercellulare, intravascolare, intraviscerale, nervoso). Si configurano così patterns di coinvolgimento topografico e temporale pressochè stereotipati tali da permettere al clinico di riconoscere nel paziente le caratteristiche morfologiche di lesioni visibili per risalire a verosimili cause. L’irradiazione parestesica pseudo-ulnare in corso di infarto del miocardio (piuttosto che la contrazione muscolare riflessa della loggia addomino-pelvica in corso di appendicite o l’attivazione iperidrosico-algida palmo-faciale in corso di ipoglicemia acuta) sono altrettanti esempi di questi “legami obbligati” la cui conoscenza empirica ha preceduto di molto le spiegazioni fisiopatologiche. In quest’ottica il modello attribuito a sir Sherrington, ovvero di una materia nervosa che si vorrebbe originata come causa prima dal riflesso integrato a livello spinale, se non perde validità in termini di realtà osservabile, risulta comunque debole dal punto di vista genealogico. Infatti il SN non prende origine dai nervi spinali (che piuttosto ne rappresentano una modalità organizzativa evolutivamente recente): esso si formò e si plasmò nell’epoca ancestrale dello sviluppo degli scambi tra sostanza intercellulare e il cosiddetto “glicocalice cellulare”, storico termine questo ormai surclassato dalle moderne conoscenze biochimiche sulle molecole di adesione intercellulari.
31l.
L’estremo opposto: la struttura patogenetica del Sistema Nervoso Centrale (SNC)
“Nella misura in cui il sistema linfatico della periferia somatica è riconosciuto quale principale effettore delle funzioni fisiologiche del liquido interstiziale, sia per quanto riguarda l’omeostasi proteica che per la sorveglianza immunitaria, l’apparente assenza di un sistema di vasi linfatici convenzionali nel Sistema Nervoso Centrale ha da sempre rappresentato un mistero delle Neuroscienze, soprattutto per l’estrema peculiare sensibilità delle cellule nervose alla composizione del loro ambiente extracellulare” [48].
Esordisce così sulla rivista “Lancet Neurology” una bellissima review del 2015 (firmata da studiosi statunitensi e danesi impegnati sui fronti della ricerca anestesiologia, neurobiologica, della Medicina Perioperatoria e Translationale) sulle conoscenze che, appena tre anni prima, avevano iniziato a comporsi sulla scoperta del “sistema gliolinfatico” [49]. La definizione di questo nuovo dispositivo biologico iniziò da allora a demolire il corpus dottrinale anatomofisiologico proposto da Lewis Hill Weed [115] che fino a pochi anni fa era dominante. Dato il ruolo della circolazione linfatica e della sua stretta relazione con competenze immunologiche il modello di Weed aveva contribuito a enfatizzare la convinzione che il SNC fosse una sorta di “santuario immunologico” in grado di proteggersi dalle noxae ambientali grazie alla “barriera ematoencefalica”. Questa concezione ha resistito a lungo nonostante l’evidente sproporzione tra l’intensa attività metabolica del SNC (foriera di altrettanto ingente produzione di scorie) e l’apparente esiguità dell’apparato preposto al suo drenaggio. Avendo già riconosciuto il destino finale degli scambi escretori del nevrasse nel drenaggio liquorale entro i collettori venosi rinoencefalici e giugulari, la teoria allora vigente non riusciva a spiegare perché in corso di eventi infiammatori encefalici non si rilevassero (come invece accade nel resto del corpo) infiltrati infiammatori a carico delle vie linfatiche direttamente connesse al deflusso venoso encefalico, ossia nelle stazioni linfonodali cervico-laterali. La scoperta del “sistema gliolinfatico” [54] ha fornito una spiegazione copernicana al problema della discrepanza tra eccesso di scorie e scarso drenaggio nel nevrasse mettendo così in ombra la vecchia immagine statico-meccanica di barriera immunologica a favore di una visione plastica e dinamica della Neuroimmunologia nella relazione tra Sistema Nervoso (SN) e ambiente. Per illustrare sommariamente come funziona il “sistema gliolinfatico” è opportuno premettere alcuni concetti fisiologici relativi al sistema linfatico extranevrassiale. Partendo dal polo arterioso fino al polo venoso, nella progressiva arborizzazione anatomica dei vasi si giunge a un estremo distale in cui le arteriole di piccolo calibro si ramificano fino ad essere rappresentate da un singolo strato uniforme di cellule endoteliali affiancate che poggiano su una lamina basale costituita da tessuto interstiziale. E’ qui che avvengono gli scambi di soluti essenziali (ossigeno, anidride carbonica, glicidi, aminoacidi e proteine) e questo livello di semplificazione vascolare è detto capillare arterioso. La pressione arteriosa indotta dalla sistole cardiaca e dalle condizioni emodinamiche regolate a livello neuroendocrino spinge il sangue attraverso la parete del capillare arterioso (endotelio) verso il tessuto interstiziale (lamina basale) in modo da filtrarne il contenuto con modalità regolate da complessi sistemi macromolecolari (pressione idraulico-osmotica). La direzione di flusso tra il tessuto interstiziale e il polo capillare successivo, quello venoso, è opposta alla precedente e avviene perché la pressione idraulico-osmotica induce un movimento di soluti dal tessuto interstiziale verso il torrente ematico. Grazie a complessi apparati biomolecolari il sistema linfatico corporeo extranevrassiale è in grado di registrare gli eccessi di filtrazione di acqua e soluti del polo arterioso rispetto alla capacità di riassorbimento da parte del polo venoso e può inserire una vera e propria pompa aspirante (il vaso linfatico) che mantiene costantemente asciutto il tessuto interstiziale. A questa funzione idraulica del vaso linfatico si associa il fatto che in tal modo (considerando la selettività dei sistemi di trasporto biomolecolare tra polo arterioso, interstizio e polo venoso) questo ulteriore drenaggio sarà maggiormente impegnato ad aspirare una serie di sostanze che tendono a ristagnare nell’interstizio per via del loro peso molecolare o per mancato riconoscimento da parte dei sistemi di trasporto posti tra interstizio ed endotelio. Tra questi “residui” annoveriamo biomolecole complesse (spesso costituenti la struttura di tossine) e strutture microbiologiche intere (virus, batteri o parassiti). A lungo è stato dato per scontato che nel SNC tali riscontri siano più rari anche se, nel caso, molto più drammatici. Ciò è tutt’altro che vero ma il pregiudizio del santuario immunologico ha anche prodotto una cronica disattenzione verso i correlati neurologici centrali delle comuni malattie annoverandoli tra gli effetti secondari di patologie d’organo. Questo probabilmente è avvenuto anche perché la risoluzione della patologia iniziale corrisponde generalmente alla scomparsa dei sintomi centrali: la dispercezione dell’ambiente circostante, la riduzione dell’equilibrio per leggera atassia cerebellare, le sensazioni di iperpatia cutanea, l’abbassamento della soglia dolorifica miofasciale, la nausea e l’inappetenza sono tutti sintomi classicamente riferibili a un impegno, seppur lieve, del SNC ma che in corso di malattie non-neurologiche (come l’influenza) sono considerate benigne e transitorie. Da ciò deriva la difficoltà che spesso si verifica in clinica di individuare in questi quadri “globali” l’eventuale sovrapposizione di patologie neurologiche propriamente dette (meningiti, ascessi cerebrali, polinevriti, polimiositi, eccetera). Invece la recente concezione del “sistema gliolinfatico” ripone al centro dell’attenzione (anche e soprattutto in Patologia) il ruolo del SNC quale dominio evolutivo superiore delle specie viventi proprio nella sua capacità di interprete del massimo livello di simbolizzazione dell’integrazione tra i flussi informazionali nervosi e quelli immuno-endocrinologici. Proviamo a spiegare meglio. L’intero contenuto del nervrasse (encefalo e midollo spinale) ripropone integralmente in scala la struttura dell’ovoide già descritto nel testo reperibile in questa stessa sezione del sito intitolato “Interazioni tra organismo e ambiente e tra settori dell’organismo” (30):
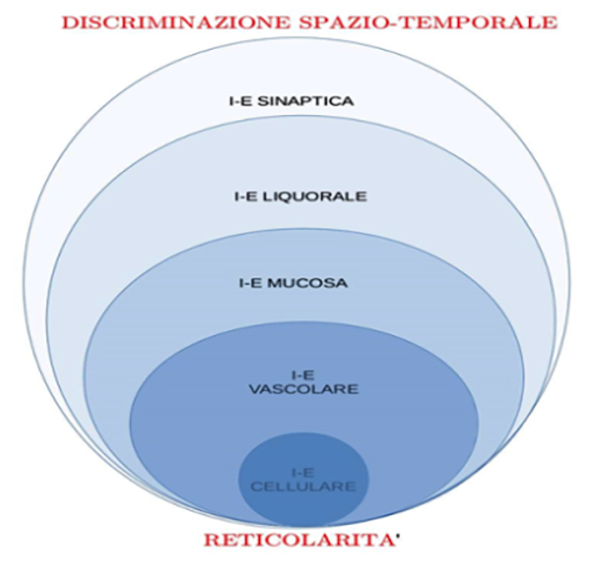
Riscontriamo infatti le interfacce di flusso intra-extracitoplasmatico, mucoso, vascolare, sieroso (liquorale) e sinaptico che si individuano nella configurazione geometrica tridimensionale in ordine alle corrispondenti strutture. Lo spazio intercellulare del parenchima nervoso è condiviso da diversi tipi di cellule, ossia i neuroni, le cellule gliali (astrociti, oligodendrociti, microgliociti) e cellule stanziali della serie ematolinfopoietica (come macrociti e mastociti). Il flusso informazionale di base tra queste unità cellulari corrisponde al trasporto di molecole nutrizionali e di svariate leve funzionali in grado di alterare localmente il ZMS. A questa comunicazione di fondo gli astrociti sovrappongono una via comunicativa preferenziale con i neuroni basata su un dispositivo bioelettrico monodirezionale: le variazioni di potenziale transmembrana del neurone vengono riversate sull’astrocita attraverso un contatto transcellulare, ossia un terminale simile a un peduncolo adeso alla superficie del neurone che trasmette passivamente all’astrocita le variazioni di concentrazione ionica della membrana neuronale [27]. Assimilabile alle gap-junction e ai desmosomi (o “sinapsi elettriche”) presenti in altri tessuti biologici, questo tipo di contatto da un lato agevola la stabilità del Potenziale di Riposo (PdR) del neurone mentre dall’altro è accoppiato alle sue funzioni escretorie tramite i processi di esocitosi mediati da enzimi dipendenti da ioni (in particolare il calcio). E’ proprio in quest’ultima funzionalità che è stata ravvisata la capacità degli astrociti di presiedere il potente sistema di “purificazione linfatica” del SNC [28]. L’Interfaccia “mucosa” individuabile nel sistema è data dal passaggio del sangue venoso attraverso i capillari del plesso coroideo. Questo assorbimento porta alla produzione di un liquido pressoché privo di cellule e macromolecole ma ricco di ioni (soluzione salina ipertonica) riversato in un compartimento capace di lambire completamente il SNC tramite il continuo passaggio da un sistema di cisterne inferiori centrali (il sistema ventricolare) a un sistema di imbibizione superiore circolare (lo spazio subaracnoideo): il liquor cerebrospinale. In altri termini, in piena autonomia il SNC produce e distribuisce al parenchima il liquido detergente con cui “lava” i suoi stessi neuroni! La circolazione del liquor cerebrospinale viene assicurata da due istanze di flusso appartenenti al dominio vascolare: la prima è quella pressoria (dominata dalla forza di eiezione cardiaca e mediata dai miociti preposti al controllo pre- e post-capillare del microcircolo), la seconda è quella endoteliale (regolata dalle interazioni molecolari col sistema intercellulare secondo il modello già descritto in “Interazioni tra organismo e ambiente” (30) e dall’integrità della sua struttura. La direzione del flusso procede quindi in modo da garantirne la continuità: l’alta pressione dei capillari arteriosi nelle diramazioni distali delle arterie encefaliche perforanti (che si approfondano nel parenchima distanziate dal compartimento intermedio rappresentato dallo spazio di Virchow-Robin) incontra l’alta resistenza dell’endotelio trasverso che si caratterizza per un forte grado di coesione cellulare longitudinale: la cosiddetta Barriera Emato-Encefalica. Nello spazio di Virchow-Robin è presente il liquor cerebrospinale che dallo spazio subaracnoideo trasuda sulla superficie della dura madre. La perfusione ad alta gittata trascina il liquor, assieme al filtrato di sangue arterioso, in prossimità del peduncolo dell’astrocita a contatto con lo strato basale subendoteliale. Mentre lo spazio intercellulare si arricchisce di ossigeno e glucosio, l’astrocita assume il liquor e lo spinge verso il neurone con cui contrae un opposto contatto peduncolare. Tramite l’astrocita il liquor assume il ruolo di assorbire attivamente le scorie del catabolismo neuronale (catene amiloidotiche, complessi proteici degenerati come le tau nell’Alzheimer, le sinucleine nel Morbo di Parkinson e patologie correlate, prioni, lipoproteine, eccetera). Una volta immesso nello spazio intercellulare, il liquor “sporco” viene drenato dal sistema capillare venoso verso due direzioni: una quota confluisce nel sistema collettore periencefalico già storicamente noto (granulazioni del Pacchioni, seni venosi, vie rino-olfattive e plesso giugulare) mentre l’altra giunge al plesso coroideo ove, a fronte della bassa pressione del capillare venoso, si dispone il già descritto sistema “mucoso” in grado di riprodurre il volume di liquor destinato alle cavità ventricolari. La bassa pressione del liquor ventricolare, che subisce ulteriori variazioni legate alla posizione antigravitaria del capo rispetto al gradiente di pressione idrostatica e agli atti ventilatori del torace, favorisce il reingresso del liquor nello spazio subaracnoideo attraverso i fori di Luschka e di Magendie del IV ventricolo. Si può così intuire come a ogni ricircolo la composizione del liquor tenda a rimanere costante e, allo stesso tempo, garantire un’efficace azione di “detersione attiva” nel suo estremo distale, ossia il neurone. Oggi perciò disponiamo di un modello dinamico di funzionamento del dominio sieroso/liquorale del sistema ove questo risulta globalmente influenzato dall’attività del descritto dispositivo gliolinfatico. Il livello superiore dell’ovoide, ovvero ciò che concerne le trasformazioni di flusso informazionale espresse dall’attività sinaptica tra neuroni coinvolti in questo ciclo di trasformazioni, è più difficile da illustrare. L’attività sinaptica dei neuroni viene misurata in due modi: da una parte attraverso la registrazione diretta della loro attività elettrica, dall’altra attraverso la misurazione (diretta o per via radiologica) del destino metabolico delle sostanze biochimiche utilizzate durante le funzioni cerebrali, siano esse cataboliti energetici o prodotti di degradazione dei neurotrasmettitori/neuromodulatori o anche precursori biochimici degli stessi. Recentissime ricerche hanno descritto una potente correlazione tra attivazione del sistema gliolinfatico e attività nervosa, in particolare rispetto alle variazioni dello stato di coscienza: è stato appurato che il sistema gliolinfatico è indotto ad attivarsi quasi esclusivamente durante il sonno e, sorprendentemente, anche durante l’anestesia generale [59]. Gli studi si sono quindi dedicati alla ricerca di un eventuale accoppiamento tra attivazione del sistema gliolinfatico e i diversi sistemi di neurotrasmissione, particolarmente quelli attivi nella modulazione del ritmo sonno-veglia, giungendo alla conclusione che il più potente e determinante è il sistema noradrenergico centrale, che dal nucleous coeruleus, si proietta a tutto il nevrasse attraverso le vie reticolari ascendenti e discendenti [82]. L’implicazione funzionale di questo rilievo è di cruciale importanza: la stessa istanza che regola i fenomeni di adattamento ambientale nelle reazioni di allerta e assolve al ruolo di coniugazione tra Sistema Nervoso e Sistema Immunitario nella periferia innervata è riconosciuta quale modulatore fondamentale dei processi autopoietici dell’ovoide con cui abbiamo fornito la rappresentazione centralizzata dell’intero organismo, ossia il nevrasse. Sul piano più strettamente fisiopatologico ulteriori speculazioni sul tema trovano spazio in questa stessa sezione del sito nel già menzionato capitolo (30), in particolare sul modello della rappresentazione centrale delle perturbazioni dei flussi informazionali nervosi e della loro capacità di attivare “dall’alto” l’infiammazione della periferia innervata [105].
Quanto al razionale terapeutico delle Terapie con Anestetici Locali (TAL) l’inserimento di un evento perturbativo aspecifico come l’applicazione di un “semplice” AL nell’interfaccia tra dominii spazio-temporali posta tra sistema sieroso-liquorale e sistema sinaptico può esprimere una specificità d’effetto maggiore rispetto a quanto ci si attende dalla somministrazione per via sistemica (diffusa perciò ubiquitariamente) di sostanze dotate soltanto di specificità recettoriale limitata al dominio sinaptico. In tal senso emerge l’estrema importanza della precisione anatomica del terapeuta che utilizza AL e si spiega l’apparente paradosso di riuscire a indurre effetti terapeutici specifici utilizzando un farmaco così spiccatamente “aspecifico”.
31m.
Riorganizzazione cronica del tessuto biologico in esito alla noxa
Fin qui abbiamo accennato alla connessione fondamentale tra la tendenza alla sensitizzazione, espressa in termini di deragliamento del rapporto tra frequenza di scarica ed entità di stimolo analogico processato in una determinata classe di neurone afferente (f/Δa x 1/T) e attivazione dei Fattori di Crescita (FdC) implicati nel rimaneggiamento dell’innervazione periferica. La combinazione di questi eventi, insorgenti a seguito di una lesione tessutale, costituisce la base elettrochimica del destino del trofismo dello tessuto danneggiato: esso potrà orientarsi verso la soluzione riparativa della cicatrizzazione oppure l’accensione di un processo reiterativo neurodistrofico più o meno localizzato. Sia che l’indirizzo riparativo conduca all’apposizione di tessuto cicatriziale sia che l’indirizzo flogistico produca la cronicizzazione della sensitizzazione fino alla sua centralizzazione (cioè alla sua ascesa verso l’alto) i livelli di integrazione nervosi immediatamente superiori alla periferia danneggiata avranno comunque inevitabilmente registrato una deformazione della geometria del campo recettoriale periferico corrispondente. In questa nuova configurazione geometrica non risulterà alterato soltanto il traffico di afferenze sensitive (con una diversa ripartizione delle priorità di rappresentazione dei settori di periferia innervata) ma anche la forma e l’estensione dei campi recettoriali stessi fino all’instaurazione di rapporti di contiguità con aree di proiezione afferenti del tutto inusuali. Un fenomeno di questo genere è molto studiato sui livelli di integrazione somato-sensitivi corticali, oggi analizzabili con metodiche scintigrafiche in vivo come la Tomografia a Emissione di Positroni (PET) e la Risonanza Magnetica Funzionale, in cui la deformazione geometrica dei campi recettoriali è riconosciuta come segno di processi plastici legati all’apprendimento o, più drammaticamente, quali conseguenze di processi di deafferentazione post-lesionale [69]. Purtroppo tutt’oggi scontiamo una notevole arretratezza tecnologica che ancora ci priva delle immagini della rappresentazione somatotopica in vivo dei livelli di integrazione nervosa più distali, quelli prossimi alla periferia innervata.
31n.
Caratteristiche morfo-funzionali della regressione cicatriziale
Assistere a un processo morboso che rapidamente vira verso la guarigione a seguito dell’infiltrazione con AL di una cicatrice ha spesso suscitato scetticismo e incredulità fino al punto di invocare l’effetto placebo se non, persino, dinamiche di suggestione. Tuttavia a ben guardare l’individuazione della cicatrice quale promotore di processi patologici innescati da un focolaio costituisce un dato che si è saldamente affermato almeno in altri due importanti settori della ricerca clinica e sperimentale: l’Epilettologia e l’Aritmologia Cardiaca (12b). Il comune denominatore di due diverse localizzazioni della cicatrice (corteccia cerebrale e miocardio) è rappresentato dalla distribuzione dell’eccitabilità che questa induce nelle citomembrane immediatamente circostanti alla zona di necrosi cellulare [22][56][61][93]. Semplificando, possiamo pensare a un modello elettrostatico di polarizzazione demarcato dai margini dell’area cicatriziale ove la polarizzazione derivi dalla contrapposizione diretta tra linee di tessuti dotate a vario titolo di caratteristiche bioelettriche (cellule, sincizi cellulari, thigh junctions, gap juctions) e strati di tessuto fibroso (in cui prevale il collagene) caratterizzato da alta resistività dielettrica. Il risultato di questo processo di ridistribuzione elettrofisiologica del tessuto è la sua possibile costituzione nel già menzionato focolaio generatore di stimoli ectopici. Sono più che evidenti le analogie di questo fenomeno con quanto altrove abbiamo illustrato circa le caratteristiche morfo-funzionali del neuroma da amputazione.
Numerose ricerche hanno tentato di identificare i meccanismi che suscitano la comparsa di un focolaio generatore di stimoli ectopici entro i processi riparativi fibrocicatriziali. C’è largo consenso nel ritenere che l’esito istologico finale sia indotto da cascate di fattori enzimatici ad azione reciprocamente opposta e alternati in base a una sequenzialità guidata da Fattori di Crescita: il mancato rispetto dell’usuale sequenzialità oppure lo squilibrio quantitativo tra fattori di opposto segno regolatorio possono indurre fenomeni cicatriziali alquanto eterogenei indipendentemente dall’entità e dall’estensione del danno tessutale d’origine. Declinato nei settori specialistici d’appartenenza (Dermatologia, Vulnologia, Chirurgia Estetica, eccetera) questo argomento conduce in un mare magnum di nozioni scaturite dalla richiesta terapeutica di contrasto allo sviluppo del cheloide, patologia tuttora contrassegnata da una sostanziale incertezza sulla sua patogenesi. In questa sede ci limitiamo a osservare come le principali e più recenti osservazioni biomolecolari sul fenomeno della predisposizione individuale a sviluppare cheloidi in seguito a eventi traumatici della cute vertano sostanzialmente sulla genetica dei Fattori di Crescita [70]. Per questa via tale concerto di eventi, di cui oggi conosciamo molti aspetti biomolecolari, diventa fonte di notevole variabilità individuale circa processi patologici globali di cui il danno tessutale iniziale assume il ruolo di innesco. Assumendo questa dimensionalità “storica” e variabile della relazione tra impatto ambientale (traumatico, infettivo, biochimico, eccetera) e la conseguente reazione tessutale endogena, l’intero processo patologico non può più essere descritto quale semplice effetto delle caratteristiche fisico-chimiche della noxa ambientale. Se ci riferiamo alla Infettivologia le interazioni tra agente infettante e ospite vedono nel primo una capacità strategica, geneticamente determinata, di colpire il secondo tramite l’instaurazione di processi patologici ma è anche vero che la sola stima della carica infettante e della sua virulenza non può predeterminare il successo dell’aggressione infettiva. In parole semplici, l’antica percezione di “predisposizione individuale” emerge con tanta più evidenza quanto più si approfondisce la componente endogena della malattia come fenomeno globale. Il fatto universalmente accettato che in Epilettologia e in Aritmologia l’impianto morfo-strutturale di una cicatrice divenga empiricamente buon motivo della sua estirpazione dovrebbe suggerirci che potrebbe risultare altrettanto utile, sul piano clinico-diagnostico, considerare il ruolo patogenetico di analoghi processi fibrocicatriziali quando si sviluppano nel derma, nel muscolo, nell’osso o sulla superficie degli organi splancnici. Il problema della trasposizione nervosa di eventi legati alla sfera del rimaneggiamento post-traumatico del trofismo tessutale, raccolti e processati in una sensorialità indistinta, ha favorito lo sviluppo di molteplici attitudini in campo terapeutico, tra cui l’Osteopatia. A questa interessante disciplina si devono utili riflessioni sui rapporti neuro-mediati (riflessi spinali e vegetativi) che si instaurano cronicamente tra periferie eterogenee (connettivi, visceri cavi e muscoli scheletrici) come fenomeni adattativi post-traumatici [110].
31o.
Razionale dell’azione della Neuromodulazione con AL sulla “malattia innervata”
Da quanto esposto sembra che oggi ci si possa liberare dal vincolo della segregazione segmentaria entro cui identificare entità morbose riconoscibili. Almeno in parte la linearità segmentale dei fenomeni morbosi è già da tempo superata dalla conoscenza delle aree di Haed [43]. Queste infatti risultano debordanti rispetto alla disposizione dermatomerica spinale e interpretate come esaltazioni delle connessioni tra afferenze sensoriali spinali e proiezioni post-gangliari delle vie neurovegetative. Il “Campo di Disturbo” (CdD) descritto dai fratelli Huneke nel corso delle applicazioni terapeutiche con AL va tuttavia molto oltre la delimitazione delle aree di Haed: l’interazione disfunzionale giunge a coprire distanze ben maggiori e distrettualità apparentemente slegate come quelle tra alveolo dentario e cingolo pelvico o tra cicatrice appendicolare e strutture meningee della base cranica. Una tale disposizione di connettività reticolare potrebbe trovare una rappresentazione unitaria solamente pensando all’integrazione su un campo recettoriale nervoso protoembrionale di epoca filo-ontogenetica. Accogliendo questa ipotesi formulata sul piano anatomo-funzionale resta da chiedersi di quale natura sia l’effetto terapeutico suscitato dall’applicazione degli Anestetici Locali (AL) sul putativo CdD. A nostro avviso vanno anzitutto scartate due spiegazioni alternative poichè prive di consistenza farmacologica e fisiopatologica: quella di un effetto farmacologico sistemico dose-dipendente e quella del ripristino di un non meglio precisato “flusso energetico”. Gli AL utilizzati nella Terapia Neurale secondo Huneke (TNH) nella “bonifica” del CdD sono semplici inibitori reversibili dei canali del sodio voltaggio-dipendenti. Ciò vuol dire che il loro impiego come farmaci iniettati al di fuori del torrente ematico si limita a inibire le comunicazioni nervose tra il tessuto periferico infiltrato e la circostante componente nervosa. L’effetto anestetico locale è assai limitato nel tempo, la farmacodinamica è lineare con gradiente dose-dipendente che coinvolge progressivamente le fibre amieliniche di piccolo calibro C (da cui la principale indicazione analgesica in Anestesiologia) fino alle fibre motorie e propriocettive di grande calibro e mielinizzate (effetto che richiede più alte concentrazioni di AL). Nella bonifica del CdD generalmente si impiegano concentrazioni non superiori all’1% incapaci di sortire alcun significativo effetto farmacologico sistemico. Ai dosaggi indicati si ottiene invece un certo grado di anestesia loco-regionale nei tessuti iniettati che corrisponde a un blocco di trasmissione da parte delle fibre afferenti di calibro più sottile. Per questo la prima ipotesi circa l’effetto terapeutico degli AL sul CdD, quella che invoca l’effetto farmacologico sistemico dose-dipendente, è da scartare. É vero che tra le tecniche iniettive previste rientrano molteplici modalità e sedi di somministrazione (tra cui anche quella siero-ematica o su centri nervosi “direzionali” come i gangli del sistema nervoso vegetativo) ma ciò non sembra avere rilevanza rispetto al fenomeno del CdD, ancor più quando la meraviglia suscitata dal successo terapeutico è connessa alla superficialità e alla modesta estensione della lesione iniettata (cicatrici cutanee, mucose, eccetera). L’altra ipotesi da scartare, che ci riporta a quanto è stato discusso in precedenza, è quella degli AL che ripristinerebbero un “flusso energetico” che il CdD avrebbe “bloccato” o ostacolato. Per quanto la spettacolarità di certi eventi curativi possa suggerire fenomeni “di liberazione” resta la sostanziale inconsistenza scientifica di tale ricostruzione che si richiama piuttosto esplicitamente ai canoni della Naturphilosophie tedesca del XIX° Secolo. In realtà l’effetto terapeutico in sé appare alquanto eterogeneo: al di là della generica scomparsa della sintomatologia dolorosa, spesso cronica intermittente-remittente, gli effetti descritti spaziano dall’incremento della perfusione di organi o distretti somatici già sotto un regime di relativa ischemia fino alla scomparsa di contratture muscolari o alla broncodilatazione (tra le più frequenti descrizioni di Fenomeno del Secondo c’è la rapida risoluzione di crisi asmatiche). Come sembra accadere nel caso degli acufeni [116] alcuni effetti prolungati dell’impiego terapeutico degli AL sono connessi allo stemperamento di fenomeni vasomotori locali.
Il modello interpretativo che qui si propone contempla che il CdD altro non sia che una disposizione casuale di un livello integrativo nervoso che assume in sé la geometria di un campo recettoriale deformato. Paradossalmente tale ipotesi trova il suo principale conforto in quella che sembra la sua maggiore apparente contraddizione: la costituzione del CdD in realtà non è affatto un meccanismo deterministico nello sviluppo di una patologia dato che questa può manifestarsi anche in forza di altre dinamiche biologiche. L’impiego terapeutico degli AL fu incoraggiato dalla constatazione empirica dell’innesto di un fenomeno di adattamento su membrane cellulari già preda di processi di sensitizzazione. La reiterazione dell’applicazione di AL equivarrebbe così alla replica di un evento informazionale di resetting della periferia innervata non dissimile dal razionale terapeutico alla base dei trattamenti elettroconvulsivanti o di cardioversione elettrica. A cavallo tra XIX° e XX° Secolo le grandi scoperte sulla fisiopatologia spinale suscitarono in molti l’idea che il SN rappresentasse poco più che il risultato della sovrapposizione di segmenti spinali e le applicazioni terapeutiche con AL restarono a lungo confinate nell’ambito segmentale. Anche se non trovarono subito il conforto di un solido background scientifico le scoperte del CdD e del Fenomeno del Secondo (FdS) “sparigliarono le carte” nel campo della applicazioni terapeutiche degli AL e, al tempo stesso, ispirarono alcune speculazioni metafisiche che ebbero l’effetto di posizionare la TNH tra le metodiche “alternative”. Il motivo per cui oggi possiamo spiegare scientificamente il FdS non può che rimanere insito nel meccanismo d’azione degli AL: essi producono una temporanea deafferentazione del campo recettoriale sovrapposto alla periferia innervata. Qualora il campo recettoriale deformato giunga a occupare aree recettoriali di livelli neuronali distanti la sua temporanea avulsione può costituire il trigger di una sua riorganizzazione altrettanto rapida e imprevedibile. In altri termini non è mai detto che nel singolo paziente il danno locale debba necessariamente ingenerare un CdD né è prevedibile se e in che modo il suo trattamento con AL possa provocare l’effetto terapeuticamente desiderato. In realtà coloro che oggi professano la TNH spesso sperimentano l’esistenza di possibili CdD nei singoli pazienti ma la loro temporanea deafferentazione con AL produce altrettanto spesso fenomeni assolutamente non terapeutici (per quanto transitori e innocenti): recrudescenze della sintomatologia dolorosa, comparsa di fenomeni vaso- o visceromotori in diversi apparati (tipiche le poliurie), quadri di ipereccitabilità neuromuscolare talora accompagnata da febbricola, eccetera. Agli occhi degli osservatori non crocifissi alla rigidità di certi criteri di validazione scientifica tale imprevedibilità, eterogeneità e difetto di “intrinseca bontà” degli eventi terapeutici mediante AL diventano più suggestivi della genuinità biologica del fenomeno anche rispetto a una disamina di efficacia condotta con i vigenti criteri “evidence based”.
[1] Alexopoulou AN, Multhaupt HA, Couchman JR
Syndecans in wound healing, inflammation and vascular biology
Int Jour Biochem Cell Biol, 39(3):505-28, 2007
[2] Ali Z, Mukwaya A, Biesemeier A, Ntzouni M, Ramsköld D, Giatrellis S et Al
Intussusceptive Vascular Remodeling Precedes Pathological Neovascularization
Arterioscler Thromb Vasc Biol, 39(7):1402-1418, Jul 2019
[3] Aloe L, Bracci-Laudiero L, Bonini S, Manni L
The expanding role of nerve growth factor: from neurotrophic activity to immunologic diseases
Allergy, 52(9):883-94, set 1997
[4] Bajusz E, Jasmin G
Skeletal Muscle Diseases: recent advances and some related basic problems
Can Med Assoc Jour, 89:555-62, Sep 1963
[5] Bano D, Ankarcrona M
Beyond the critical point: An overview of excitotoxicity, calcium overload and the downstream consequences
Neurosci Lett, 10;663:79-85, Jan 2018
[6] Bastide M, Bordet R, Pu Q, Robin E, Puisieux F, Dupuis B
Relationship between inward rectifier potassium current impairment and brain injury after cerebral ischemia/reperfusion
Jour Cereb Blood Flow Metab, 19(12):1309-15, Dec 1999
[7] Belluzzi E, Stocco E, Pozzuoli A, Granzotto M, Porzionato A, Vettor R, De Caro R, Ruggieri P et Al
Contribution of Infrapatellar Fat Pad and Synovial Membrane to Knee Osteoarthritis Pain
Biomed Res Int, 6390182, Mar 2019
[8] Berić A
Central pain: “new” syndromes and their evaluation
Muscle Nerve, 16(10):1017-24, Oct 1993
[9] Betancourt BAP, Florczyk SJ, Simon M, Juba D, Douglas JF, Keyrouz W, Bajcsy P, Lee C, Simon CG
Effect of the scaffold microenvironment on cell polarizability and capacitance determined by probabilistic computations
Biomed Mater, 13(2):025012, Jan 30 2018
[10] Bhattacharyya S, Tobacman JK
Hypoxia reduces arylsulfatase B activity and silencing arylsulfatase B replicates and mediates the effects of hypoxia
PLoS One, 7(3):e33250, 2012
[11] Bijlard E, Uiterwaal L, Kouwenberg CA, Mureau MA, Hovius SE, Huygen FJA
Systematic Review on the Prevalence, Etiology, and Pathophysiology of Intrinsic Pain in Dermal Scar Tissue
Pain Physician, 20(2):1-13, Feb 2017
[12] Bonica JJ
Evolution and current status of pain programs
Jour Pain Symptom Manage, 5(6):368-74, Dec 1990
[13] Bray N
Sensory transduction: Merkel cells bring a delicate touch
Nat Rev Neurosci, 15(6):348-9, Jun 2014
[14] Breward J, Gentle MJ
Neuroma formation and abnormal afferent nerve discharges after partial beak amputation (beak trimming) in poultry
Experientia, 41(9):1132-4, Sep 1985
[15] Brown MC, Hopkins WG
Role of degenerating axon pathways in regeneration of mouse soleus motor axons
Jour Physiol, 318:365-73, Sep 1981
[16] Bussa M, Guttilla D, Lucia M, Mascaro A, Rinaldi S
Complex regional pain syndrome type I: a comprehensive review
Acta Anaesthesiol Scand, 59(6):685-97, Jul 2015
[17] Campero M, Serra J, Marchettini P, Ochoa JL
Ectopic impulse generation and autoexcitation in single myelinated afferent fibers
in patients with peripheral neuropathy and positive sensory symptoms
Muscle Nerve, 21(12):1661-7, Dec 1998
[18] Cerveró F
Neurobiology of pain
Rev Neurol, 30(6):551-5, Mar 2000
[19] Chen Z, Chen X, Liu M, Dong Z, Ma L, Yu S
Altered functional connectivity architecture of the brain in medication overuse headache using resting state fMRI
Jour Headache Pain, 18:25, 2017
[20] Chéry-Croze S
Painful sensation induced by a thermal cutaneous stimulus
Pain, 17(2):109-3, Oct 1983
[21] Coderre TJ, Katz J
Peripheral and central hyperexcitability: differential signs and symptoms in persistent pain
Behav Brain Sci, 20(3):404-19, Sep 1997
[22] Colin D, Caig MC, Rajnicek AM, Song B, Zhao M
Controlling Cell Behavior Electrically: Current Views and Future Potential
Physiol Rev, 85:943–978, 2005
[23] Culp WJ, Ochoa J, Cline M, Dotson R
Heat and mechanical hyperalgesia induced by capsaicin. Cross modality threshold modulation in human C nociceptors
Brain, 112(Pt 5):1317-31, Oct 1989
[24] Devor M, Schonfeld D, Seltzer Z, Wall PD
Two modes of cutaneous reinnervation following peripheral nerve injury
Jour Comp Neurol, 185(1):211-20, May 1979
[25] Devor M, Wall PD, Catalan N
Systemic lidocaine silences ectopic neuroma and DRG discharge without blocking nerve conduction
Pain, 48(2):261-8, Feb 1992
[26] Diamond J, Foerster A
Recovery of sensory function in skin deprived of its innervation by lesion of the peripheral nerve
Exp Neurol, 115(1):100-3, Jan 1992
[27] Ding F, O’Donnell J, Xu Q, Kang N, Goldman N, Nedergaard M
Changes in the composition of brain interstitial ions control the sleep-wake cycle
Science, 352(6285):550-555, 2016
[28] DiNuzzo M, Nedergaard M
Brain energetics during the sleep-wake cycle
Curr Opin Neurobiol, 47:65-72, 2017
[29] Elson E
II. Model building: an electrical theory of control of growth and development in animals,
prompted by studies of exogenous magnetic field effects (paper I), and evidence of DNA current conduction, in vitro
Electromagn Biol Med, 28(3):283-309, 2009
[30] Ersoy H, Pomeranz SJ
Complex Regional Pain Syndrome
Jour Surg Orthop Adv, 25(2):117-20, 2016
[31] Farber PL, Hochman B, Furtado F, Ferreira LM
Electricity and colloidal stability: how charge distribution in the tissue can affects wound healing
Med Hypotheses, 82(2):199-204, Feb 2014
[32] Fenton BW, Shih E, Zolton J
The neurobiology of pain perception in normal and persistent pain
Pain Manag, 5(4):297-317, 2015
[33] Ferguson MW, O’Kane S
Scar-free healing: from embryonic mechanisms to adult therapeutic intervention
Philos Trans R Soc Lond B Biol Sci, 359(1445):839-50, May 2004
[34] Fernández-de-Las-Peñas C
Myofascial Head Pain
Curr Pain Headache Rep, 19(7):28, Jul 2015
[35] Fischer E
Changes in protein and enzymes in muscular degeneration subsequent to denervation
Am Jour Phys Med, 34(1):212-22, 1955
[36] Fitzgerald M
The spread of sensitization of polymodal nociceptors in the rabbit from nearby injury and by antidromic nerve stimulation
Jour Physiol, 297:207-16, Dec 1979
[37] Freeman TA, Parvizi J, Della Valle CJ, Steinbeck MJ
Reactive oxygen and nitrogen species induce protein and DNA modifications driving arthrofibrosis following total knee arthroplasty
Fibrogenesis Tissue Repair, 2(1):5, Nov 2009
[38] Gehrmann J, Monaco S, Kreutzberg GW
Spinal cord microglial cells and DRG satellite cells rapidly respond to transection of the rat sciatic nerve
Restor Neurol Neurosci, 2(4):181-98, Jan 1991
[39] Goerges AL, Nugent MA
Regulation of vascular endothelial growth factor binding and activity by extracellular pH
Jour Biol Chem, 278(21):19518-25, May 2003
[40] Goldstein RS, Raber P, Govrin-Lippmann R, Devor M
Contrasting time course of catecholamine accumulation and of spontaneous discharge in experimental neuromas in the rat
Neurosci Lett, 94(1-2):58-63, Nov 1988
[41] Grodzinsky AJ
Electromechanical and physicochemical properties of connective tissue
Crit Rev Biomed Eng, 9(2):133-99, 1983
[42] Hart FX
Cytoskeletal forces produced by extremely low-frequency electric fields acting on extracellular glycoproteins
Bioelectromagnetics, 31(1):77-84, 2010
[43] Head H
On disturbances of sensation with especial reference to the pain of visceral disease
Brain, 16:1-133, 1893
[44] Hermanns H, Hollmann MW, Stevens MF, Lirk P, Brandenburger T, Piegeler T, Werdehausen R
Molecular mechanisms of action of systemic lidocaine in acute and chronic pain: a narrative review
Brit Jour Anaesth, 123(3):335-349, Sept 2019
[45] Hirth M, Rukwied R, Gromann A, Turnquist B, Weinkauf B, Francke K, Albrecht P, Rice F, Hägglöf B et Al
Nerve growth factor induces sensitization of nociceptors without evidence for increased intraepidermal nerve fiber density
Pain, 154(11):2500-1, Nov 2013
[46] Hronik-Tupaj M, Kaplan DL
A review of the responses of two- and three-dimensional engineered tissues to electric fields
Tissue Eng Part B Rev, 18(3):167-80, Jun 2012
[47] Hu P, McLachlan EM
Long-term changes in the distribution of galanin in dorsal root ganglia after sciatic or spinal nerve transection in rats
Neuroscience, 103(4):1059-71, 2001
[48] Iliff JJ, Goldman SA, Maiken Nedergaard M
Clearing the mind: Implications of dural lymphatic vessels for brain function
Lancet Neurol, 14(10):977–979, Oct 2015
[49] Iliff JJ, Wang M, Liao Y et Al
A paravascular pathway facilitates CSF flow through the brain parenchyma
and the clearance of interstitial solutes, including amyloid β
Sci Transl Med, 4(147):147ra111, 2012
[50] Jänig W
Activation of afferent fibers ending in an old neuroma by sympathetic stimulation in the rat
Neurosci, 111(3):309-14, Apr 1990
[51] Jänig W
Spinal cord reflex organization of sympathetic systems
Prog Brain Res, 107:43-77, 1996
[52] Jänig W
Sympathetic nervous system and pain: ideas, hypotheses, models
Schmerz, 7(4):226-40, Dec 1993
[53] Jänig W, Levine JD, Michaelis M
Interactions of sympathetic and primary afferent neurons following nerve injury and tissue trauma
Prog Brain Res, 113:161-84, 1996
[54] Jessen NA, Munk AS, Lundgaard I, Nedergaard M
The Glymphatic System: A Beginner’s Guide
Neurochem Res, 40(12):2583-2599, 2015
[55] Jørum E, Ørstavik K, Schmidt R, Namer B, Carr RW, Kvarstein G, Hilliges M, Handwerker H, Torebjörk E, Schmelz M
Catecholamine-induced excitation of nociceptors in sympathetically maintained pain
Pain, 127(3):296-301, Feb 2007
[56] Josephson ME, Wellens HJ
Electrophysiologic evaluation of supraventricular tachicardia
Cardiol Clin, 15(4):567-86, 1997
[57] Kennedy WR, Sakuta M
Collateral reinnervation of sweat glands
Ann Neurol, 15(1):73-8, Jan 1994
[58] Kincaid W, Neubert MJ, Xu M, Kim CJ, Heinricher MM
Role for medullary pain facilitating neurons in secondary thermal hyperalgesia
Jour Neurophysiol, 95(1):33-41, Jan 2006
[59] Kjaerby C, Rasmussen R, Andersen M, Nedergaard M
Does Global Astrocytic Calcium Signaling Participate in Awake Brain State Transitions and Neuronal Circuit Function?
Neurochem Res, 42(6):1810-1822, 2017
[60] Kobayashi H, Mizisin AP
Nerve growth factor and neurotrophin-3 promote chemotaxis of mouse macrophages in vitro
Neurosci Lett, 305(3):157-60, Jun 2001
[61] Lee RC, Canaday DJ, Doong H
A review of the biophysical basis for the clinical application of electric fields in soft-tissue repair
Jour Burn Care Rehabil, 14(3):319-35, May–Jun 1993
[62] Lekan HA, Chung K, Yoon YW, Chung JM, Coggeshall RE
Loss of dorsal root ganglion cells concomitant with dorsal root axon sprouting following segmental nerve lesions
Neuroscience, 81(2):527-34, Nov 1997
[63] Leriche R
Algies ascendantes post-traumatiques spécialement après opérations sur les doigts
Praxis, 35(51-52):885, Dec 1946
[64] Lin CS, Mogyoros I, Kuwabara S, Cappelen-Smith C, Burke D
Differences in responses of cutaneous afferents in the human median and sural nerves to ischemia
Muscle Nerve, 24(11):1503-9, Nov 2001
[65] Lu X, Richardson PM
Responses of macrophages in rat dorsal root ganglia following peripheral nerve injury
Jour Neurocytol, 22(5):334-4, May 1993
[66] Mao J, Chen LL
Systemic Lidocaine for Neuropathic Pain Relief
Pain, 87:7-17, 2000
[67] Maehlen J, Njå A
Selective synapse formation during sprouting after partial denervation of the guinea-pig superior cervical ganglion
Jour Physiol, 319:555-67, 1981
[68] Maeyashiki T, Jang JH, Janker F, Yamada Y, Inci I, Weder W, Piegeler T, Jungraithmayr W
The Amide Local Anesthetic Ropivacaine Attenuates Acute Rejection After Allogeneic Mouse Lung Transplantation
Lung, 197(2):217-226, Apr 2019
[69] Martinez-Ferrer M, Afshar-Sherif A-R, Uwamariya C, de Crombrugghe B, Davidson JM, Bhowmick NA
Dermal Transforming Growth Factor-β Responsiveness Mediates Wound Contraction and Epithelial Closure
Am Jour Pathol, 176(1):98–107, Jan 2010
[70] Maihöfner C, Nickel FT, Seifert F
Neuropathic pain and neuroplasticity in functional imaging studies
Schmerz, 24(2):137-45, Apr 2010
[71] Malone K, Amu S, Moore AC, Waeber C
Immunomodulatory Therapeutic Strategies in Stroke
Front Pharmacol, 10:630, Jun 2019
[72] Matas M, Sotošek V, Kozmar A, Likić R, Sekulić A
Effect of local anesthesia with lidocaine on perioperative proinflammatory cytokine levels
in plasma and cerebrospinal fluid in cerebral aneurysm patients: Study protocol for a randomized clinical trial
Medicine (Baltimore), 98(42):e17450, Oct 2019
[73] McCaig CD, Rajnicek AM, Song B, Zhao M
Controlling cell behavior electrically: current views and future potential
Physiol Rev, 85(3):943-78, Jul 2005
[74] McLachlan EM, Jänig W, Devor M, Michaelis M
Peripheral nerve injury triggers noradrenergic sprouting within dorsal root ganglia
Nature, 363(6429):543-6, Jun 1993
[75] Merskey H
Logic, truth and language in concepts of pain
Qual Life Res, 3(Suppl 1):S69-76, Dec 1994
[76] Messlinger K, Balcziak LK, Russo AF
Cross-talk signaling in the trigeminal ganglion: role of neuropeptides and other mediators
Jour Neural Transm (Vienna), Feb 2020
[77] Mukandala G, Tynan R, Lanigan S, O’Connor JJ
The Effects of Hypoxia and Inflammation on Synaptic Signaling in the CNS
Brain Sci, 6(1):6, Mar 2016
[78] Murrell GA
Scientific Comment. Basic Science of Dupuytren’s Disease
Ann Chir Main Memb Super, 11(5):355-61, 1992
[79] Nesterkina M, Kravchenko I
Analgesic Activity of Novel GABA Esters after Transdermal Delivery
Nat Prod Commun, 11(10):1419-1420, Oct 2016
[80] Neumann S, Doubell TP, Leslie T, Woolf CJ
Inflammatory pain hypersensitivity mediated by phenotypic switch in myelinated primary sensory neurons
Nature, 384(6607):360-4, Nov 1996
[81] Noguchi K, Kawai Y, Fukuoka T, Senba E, Miki K
Substance P induced by peripheral nerve injury in primary afferent sensory neurons
and its effect on dorsal column nucleus neurons
Jour Neurosci, 15(11):7633-43, Nov 1995
[82] O’Donnell J, Ding F, Nedergaard M
Distinct functional states of astrocytes during sleep and wakefulness:
Is norepinephrine the master regulator?
Curr Sleep Med Rep, 1(1):1-8, 2015
[83] Ochoa JL, Torebjörk HE
Paraesthesiae from Ectopic Impulse Generation in Human Sensory Nerves
Brain, 103(4):835-53, Dec 1980
[84] Oishi Y, Manabe I
Macrophages in inflammation, repair and regeneration
Int Immunol, 30(11):511-528, Oct 2018
[85] Okuse K, Chaplan SR, McMahon SB, Luo ZD, Calcutt NA, Scott BP, Akopian AN, Wood JN
Regulation of expression of the sensory neuron-specific sodium channel SNS in inflammatory and neuropathic pain
Mol Cell Neurosci, 10(3-4):196-207, 1997
[86] Pertens E, Urschel-Gysbers BA, Holmes M, Pal R, Foerster A, Kril Y, Diamond J
Intraspinal and behavioral consequences of nerve growth factor-induced nociceptive sprouting
and nerve growth factor-induced hyperalgesia compared in adult rats
Jour Comp Neurol, 410(1):73-89, Jul 1999
[87] Pette D, Vrbová G
Neural control of phenotypic expression in mammalian muscle fibers
Muscle Nerve, 8(8):676-89, Oct 1985
[88] Pichert A, Samsonov SA, Theisgen S, Thomas L, Baumann L, Schiller J, Beck-Sickinger AG, Huster D, Pisabarro MT
Characterization of the interaction of interleukin-8 with hyaluronan, chondroitin sulfate, dermatan sulfate
and their sulfated derivatives by spectroscopy and molecular modeling
Glycobiology, 22(1):134-45, Jan 2012
[89] Pischinger A
Das System der Grundregulation. Grundlagen für eine ganzheitsbiologische Theorie der Medizin
Heidelberg, 1975
[90] Piro M, Giubilato G, Pinnelli M, Giordano Sciacca P, Biasucci LM
Endothelium and inflammation
Panminerva Med, 47(2):75-80, Jun 2005
[91] Raghavan S, Bitar KN
The influence of extracellular matrix composition on the differentiation of neuronal subtypes
in tissue engineered innervated intestinal smooth muscle sheets
Biomaterials, 35(26):7429-40, Aug 2014
[92] Rao RM, Yang L, Garcia-Cardena G, Luscinskas FW
Endothelial-dependent mechanisms of leukocyte recruitment to the vascular wall
Circ Res, 101(3):234-47, Aug 2007
[93] Redecker C, Lutzenburg M, Gressens P, Evrard P, Witte OW, Hagemann G
Excitability changes and glucose metabolism in experimentally induced focal cortical dysplasias
Cereb Cortex, 8(7):623-34, Oct–Nov 1998
[94] Rinaldi PC, Young RF, Albe-Fessard D, Chodakiewitz J
Spontaneous neuronal hyperactivity in the medial and intralaminar thalamic nuclei of patients with deafferentation pain
Jour Neurosurg, 74(3):415-21, Mar 1991
[95] Sahai S, McFarland R, Skiles ML, Sullivan D, Williams A, Blanchette JO
Tracking hypoxic signaling in encapsulated stem cells
Tissue Eng Part C Methods, 18(7):557-65, Jul 2012
[96] Schaible HG, Schmidt RF, Willis WD
Enhancement of the responses of ascending tract cells in the cat spinal cord by acute inflammation of the knee joint
Exp Brain Res, 66(3):489-99, 1987
[97] Schreiber RC, Krivacic K, Kirby B, Vaccariello SA, Wei T, Ransohoff RM, Zigmond RE
Monocyte chemoattractant protein (MCP)-1 is rapidly expressed by sympathetic ganglion neurons following axonal injury
Neuroreport, 12(3):601-6, Mar 2001
[98] Schreiber RC, Shadiack AM, Bennett TA, Sedwick CE, Zigmond RE
Changes in the macrophage population of the rat superior cervical ganglion after postganglionic nerve injury
Jour Neurobiol, 27(2):141-53, Jun 1995
[99] Schwartz L, da Veiga Moreira J, Jolicoeur M
Physical forces modulate cell differentiation and proliferation processes
Jour Cell Mol Med, 22(2):738-745, Feb 2018
[100] Seyrek E, Dubin P
Glycosaminoglycans as Polyelectrolytes
Adv Colloid Interface Sci, 158(1-2):119-29, Jul 2010
[101] Smith ML Jr, Adrian EK Jr
On the presence of mononuclear leucocytes in dorsal root ganglia following transection of the sciatic nerve
Anat Rec, 172(3):581-7, Mar 1972
[102] Song XJ, Hu SJ, Greenquist KW, Zhang JM, LaMotte RH
Mechanical and thermal hyperalgesia and ectopic neuronal discharge after chronic compression of dorsal root ganglia
Jour Neurophysiol, 82(6):3347-58, Dec 1999
[103] Sorg H, Tilkorn DJ, Mirastschijski U, Hauser J, Kraemer R
Panta Rhei: Neovascularization, Angiogenesis and Nutritive Perfusion in Wound Healing
Eur Surg Res, 59(3-4):232-241, 2018
[104] Sotgiu ML, Lacerenza M, Marchettini P
Effect of systemic lidocaine on dorsal horn neuron hyperactivity following chronic peripheral nerve injury in rats
Somatosens Mot Res, 9(3):227-33, 1992
[105] Speransky AD
Grundlagen der Theorie der Medizin
Leningrad, 1934 (Übersetzung der 3. Aufl., Berlin 1950)
[106] Spray DC, Hanani M
Gap junctions, pannexins and pain
Neurosci Lett, 695:46-52, Mar 2019
[107] Storozhuk MV, Moroz OF, Zholos AV
Multifunctional TRPV1 Ion Channels in Physiology and Pathology with Focus on the Brain, Vasculature, and Some Visceral Systems
Biomed Res Int, 2019:5806321, May 2019
[108] Strichartz GR, Zhou Z, Sinnott C, Khodorova A
Therapeutic concentrations of local anaesthetics unveil the potential role of sodium channels in neuropathic pain
Novartis Found Symp, 241:189-201, 2002
[109] Trouvin AP, Perrot S
New concepts of pain
Best Pract Res Clin Rheumatol, 33(3):101415, Jun 2019
[110] Van Buskirk RL
Nociceptive reflexes and the somatic dysfunction: a model
Jour Am Osteopath Assoc, 90(9):792-4, 797-809, Sept 1990
[111] van Welie I, van Hooft JA, Wadman WJ
Homeostatic scaling of neuronal excitability by synaptic modulation of somatic hyperpolarization-activated Ih channels
Biol Sci, 101(14):5123-5128, Mar 2004
[112] Vishnevsky VA
Die Technik der Novocainblockade des Sympathicus im Lendenbereich
Arch Biol Wissensch, 4:519-520, 1933
[113] Wallace R
Metabolic Free Energy and Biological Codes: A ‘Data Rate Theorem’ Aging Model
Bull Math Biol, 77(6):879-903, Jun 2015
[114] Waxman SG
The molecular pathophysiology of pain: abnormal expression of sodium channel genes and its contributions to hyperexcitability of primary sensory neurons
Pain, Suppl 6:S133-40, Aug 1999
[115] Weed LH
Studies on Cerebro-Spinal Fluid. No. III: The pathways of escape from the Subarachnoid Spaces with particular reference to the Arachnoid Villi
Jour Med Res, 31(1):51-91, 1914
[116] Weinmeister KP
Prolonged suppression of tinnitus after peripheral nerve block using bupivacaine and lidocaine
Reg Anesth Pain Med, 25(1):67-68, Jan–Feb 2000
[117] Willis W
Dorsal root potentials and dorsal root reflexes: a double-edged sword
Exp Brain Res, 4:395–421, 1999
[118] Yao L, Li Y
The Role of Direct Current Electric Field-Guided Stem Cell Migration in Neural Regeneration
Stem Cell Rev Rep, 12(3):365-75, Jun 2016
[119] Yunus MB
Editorial review: an update on central sensitivity syndromes and the issues of nosology and psychobiology
Curr Rheumatol Rev, 11(2):70-85, 2015
[120] Zhang MD, Su J, Adori C, Cinquina V, Malenczyk K, Girach F, Peng C, Ernfors P, Löw P, Borgius L et Al
Ca2+-binding protein NECAB2 facilitates inflammatory pain hypersensitivity
Jour Clin Invest, 128(9):3757-3768, Aug 2018
[121] Zhou J, Yue D, Bai Y, Kong F, Pan J
Map and correlate intracellular calcium response and matrix deposition in cartilage under physiological oxygen tensions
Jour Cell Physiol, 233(6):4949-4960, Jun 2018
[122] Zhou XF, Rush RA
Endogenous nerve growth factor is required for regulation of the low affinity neurotrophin receptor (p75) in sympathetic but not sensory ganglia
Jour Comp Neurol, 372(1):37-48, Aug 1996



